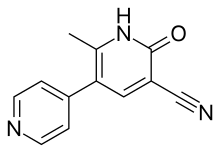
Un inhibidor de PDE3 es un fármaco que inhibe la acción de la enzima fosfodiesterasa PDE3 . Se utilizan para la terapia de insuficiencia cardíaca aguda y shock cardiogénico .
Usos médicos [ editar ]
Cardíaco [ editar ]
La amrinona , milrinona y enoximona se utilizan clínicamente para el tratamiento a corto plazo de la insuficiencia cardíaca en presencia de shock cardiogénico. [1]
Los inhibidores de PDE3 están indicados como inotrópicos para el tratamiento de la insuficiencia cardíaca aguda si las catecolaminas son ineficaces. [2] Estudios bien controlados han demostrado que estos medicamentos generalmente aumentan la mortalidad , [3] cuando se usan para el tratamiento de la insuficiencia cardíaca aguda, por lo que deben aplicarse bajo una estrecha observación. [1]
Enfermedad de las arterias periféricas [ editar ]
El cilostazol se usa para el tratamiento de la claudicación intermitente . Este fármaco tiene un efecto inotrópico positivo mucho más débil que los fármacos utilizados para el tratamiento de la insuficiencia cardíaca aguda y carece de efectos cardíacos adversos significativos. [4]
Contraindicaciones [ editar ]
Cardíaco [ editar ]
Las contraindicaciones son miocardiopatía obstructiva grave , hipovolemia , taquicardia y aneurisma ventricular . La lactancia está prohibida durante el tratamiento. [1]
Efectos adversos [ editar ]
Cardíaco [ editar ]
Los efectos adversos más importantes cuando se utiliza para el tratamiento de la insuficiencia cardíaca aguda son arritmia , trombocitopenia y aumento de los niveles de transaminasas . [1] [2]
Tipos [ editar ]
Los inhibidores de PDE3 aprobados incluyen los siguientes:
- amrinona
- cilostazol
- milrinona
- enoximona
- pimobendan (aprobado para su uso en perros)
Mecanismo de acción [ editar ]
Los inhibidores de PDE3 son un tipo de inhibidores de la fosfodiesterasa . La inhibición de la isoenzima 3 de la PDE conduce a un aumento de las concentraciones intracelulares del segundo mensajero monofosfato cíclico de adenosina (cAMP). AMPc media la fosforilación de proteína quinasas , que a su vez activa los canales de calcio cardíacos . Un aumento de la entrada de calcio desde el retículo sarcoplásmico (SR) durante la fase 2 (la fase de meseta) del potencial de acción cardíacoconduce a un efecto inotrópico positivo de los inhibidores de PDE3: aumentan la fuerza de contracción cardíaca. El aumento del reflujo de calcio en el SR después de la fase de meseta es responsable de su efecto lusitrópico positivo : aumentan la velocidad de relajación. Además, los inhibidores de PDE3 actúan como vasodilatadores . [1] [2]
Propiedades químicas [ editar ]
Inhibidores de PDE3 de primera generación [ editar ]
El reconocimiento de que el conocimiento sobre la PDE podría usarse para desarrollar fármacos que fueran inhibidores de la PDE condujo a una extensa investigación. La mayoría de los estudios utilizaron análogos de los sustratos de nucleótidos o derivados de inhibidores de productos naturales como la xantina (por ejemplo, teofilina ) y papaverina . [5] [6]
El sitio activo de PDE3 puede considerarse como un resumen de las ideas sobre la topografía del receptor resultante de los inhibidores de primera generación. El modelo de Wells et al. La versión citada en Erhardt y Chou (1991) incluye lo siguiente:
- Un área de unión de fosfato
- Un área lipofílica que acomoda el lado no polar del resto de ribosa.
- Un sitio de unión de pirimidina
- Una porción del sitio de unión de imidazol del sitio de unión de pirimidina
- Un sitio estéricamente impedido
- Un área con tolerancia a granel [5]
Inhibidores de PDE3 de segunda generación [ editar ]
Desde que se reconoció que los inhibidores selectivos de PDE3 son fármacos cardiotónicos , ha habido un gran interés en desarrollar nuevos fármacos de esta categoría. Se ha sintetizado una gran cantidad de compuestos heterocíclicos durante investigaciones relacionadas. Estos compuestos constituyen una segunda generación de inhibidores de PDE. Aunque se han dirigido principalmente a PDE3, presentan una relación estructura-actividad significativa para las PDE en general. [5]
Se ha considerado necesario un patrón de "heterociclo-fenil-imidazol" (HPI) para una actividad inotrópica positiva en el músculo cardíaco y muchos inhibidores de segunda generación se ajustan a este patrón. [5]
La región del heterociclo : dentro de cada heterociclo existe la presencia de un dipolo y un protón ácido adyacente (una función amida). Se cree que estos átomos imitan el centro electrófilo en el grupo fosfato en cAMP y se confirma como el sitio principal de unión. El heterociclo es un inhibidor análogo del estado de transición de la PDE. Los grupos alquilo , limitados a metilo o etilo , en el anillo heterocíclico generalmente mejoran la potencia, con excepciones ocasionales. [5] [6]
La región del fenilo : parece que debe estar presente un centro rico en electrones, como el fenilo . Los efectos beneficiosos de los pequeños grupos alquilo en el heterociclo podrían consistir en desviar el anillo central de la coplanariedad exacta con el anillo heterocíclico. Existe un giro similar en el AMPc y existe un acuerdo general de que los inhibidores de PDE3 de alta afinidad deberían adoptar una conformación plana favorecida energéticamente que imita la conformación anti del AMPc. [5] [6]
La región de imidazol : se han colocado varios sustituyentes en la posición para del anillo de fenilo central. Son restos ricos en electrones y aparentemente no se puede tolerar un resto cargado positivamente en esta región del receptor de PDE. Existe un acuerdo general sobre la potencia de este inhibidor: lactama ≥ alquil-CONH- ≥ imidazoilo = piridina en lugar del fenilo central con su nitrógeno en la posición 4 análoga ≥ alquil-S-> éter simple > haluro = amina > imidazolio (que es totalmente inactivo). [5]
La identificación de características comunes a los inhibidores más selectivos ha llevado a un "modelo de cinco puntos" con:
- Presencia de un dipolo fuerte ( resto carbonilo ) en un extremo de la molécula.
- Un protón ácido adyacente.
- Un sustituyente alquilo de tamaño pequeño en el anillo heterocíclico.
- Una topografía general relativamente plana.
- Un centro rico en electrones y / o un sitio aceptor de enlace de hidrógeno opuesto al dipolo. [6]
Ejemplos de inhibidores selectivos de PDE3 [ editar ]
Esta sección puede requerir una limpieza para cumplir con los estándares de calidad de Wikipedia . ( Junio de 2010 ) ( Obtenga información sobre cómo y cuándo eliminar este mensaje de plantilla ) |
Teofilina , un inhibidor no selectivo | Meribendan , un inhibidor altamente selectivo |
La teofilina es un agente no selectivo. Por el contrario, el meribendan es un inhibidor altamente selectivo. [6]
Además, el meribendan tiene un mayor nivel de selectividad en comparación con el compuesto original CI-930 porque, además del nitrógeno básico adyacente al resto de lactama, posee otro nitrógeno básico (anillo de bencimidazol), opuesto al sitio de unión primario. [6]
Investigación [ editar ]
RPL-554 es un análogo de la trequinsina y, al igual que la trequinsina, es un inhibidor dual de las enzimas fosfodiesterasas PDE-3 y PDE-4. [7] En octubre de 2015, el RPL-554 inhalado administrado a través de un nebulizador estaba en desarrollo para la EPOC y se había estudiado en el asma. [8]
Referencias [ editar ]
- ^ a b c d e Mutschler, Ernst; Schäfer-Korting, Monika (1997). Arzneimittelwirkungen (en alemán). Stuttgart: Wissenschaftliche Verlagsgesellschaft. págs. 454–455, 496.
- ^ a b c Adelante; Henschler; Rummel (2002). Allgemeine und spezielle Pharmakologie und Toxikologie (en alemán). Munich. pag. 457.
- ^ "Aprobación de Cilostazol" . FDA. 25 de septiembre de 2006. Archivado desde el original el 27 de abril de 2007.
- ^ Yan, Chen. "Regulación de la Fosfodiesterasa 3 y el Represor Temprano de AMPc inducible en el corazón" . Investigación de circulación . Consultado el 23 de enero de 2016 .
- ^ a b c d e f g Erhardt PW; Chou Y. (1991). "Un modelo topográfico para el sitio activo de c-AMP fosfodiesterasa III". Ciencias de la vida, 49 (8): 553-568.
- ^ a b c d e f Fossa P .; Boggia R .; Mosti L. (1998). "Hacia la identificación del sitio catalítico de fosfodiesterasa inhibida de cGMP cardíaco". Revista de diseño molecular asistido por computadora, 12 (4): 361-372.
- ^ Boswell-Smith V y col. La farmacología de dos nuevos inhibidores de la fosfodiesterasa 3/4 de acción prolongada, RPL554 [9,10-dimetoxi-2 (2,4,6-trimetilfenilimino) -3- (n-carbamoil-2-aminoetil) -3,4,6 , 7-tetrahidro-2H-pirimido [6,1-a] isoquinolin-4-ona] y RPL565 [6,7-dihidro-2- (2,6-diisopropilfenoxi) -9,10-dimetoxi-4H-pirimido [ 6,1-a] isoquinolin-4-ona]. J Pharmacol Exp Ther. Agosto de 2006; 318 (2): 840-8. PMID 16682455
- ^ Nick Paul Taylor para FierceBiotech. 1 de octubre de 2015 Verona pone la mira en PhIIb después de que el fármaco para la EPOC pase por un ensayo inicial