La pirazolona es un heterociclo de 5 miembros que contiene dos átomos de nitrógeno adyacentes . Puede verse como un derivado del pirazol que posee un grupo carbonilo adicional (C = O). Los compuestos que contienen este grupo funcional son útiles comercialmente en analgésicos y colorantes. [1]
Estructura y síntesis [ editar ]
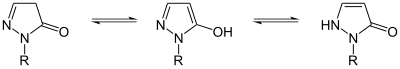
La pirazolona puede existir en dos isómeros: 3-pirazolona y 4-pirazolona.
Estos isómeros pueden interconvertirse mediante tautomería de lactama-lactima e imina-enamina ; estas conversiones a menudo muestran fotocromismo . Para los derivados de pirazolona, el isómero 3-pirazolona se puede estabilizar con sustituyentes N- alquilo o N -arilo.
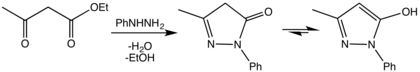
La primera síntesis de pirazolonas fue reportada en 1883 por Ludwig Knorr , mediante una reacción de condensación entre acetoacetato de etilo y fenilhidrazina . [2]
Muchas pirazolonas se producen mediante funcionalización de pirazolonas preformadas.
Aplicaciones [ editar ]
Productos farmacéuticos [ editar ]
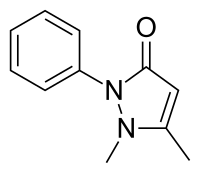
Las pirazolonas se encuentran entre los productos farmacéuticos sintéticos más antiguos, comenzando con la introducción de la antipirina (fenazona) en la década de 1880. [3] [4] Los compuestos generalmente actúan como analgésicos e incluyen dipirona (metamizol), aminopirina , ampirona , famprofazona , morazona , nifenazona , piperylon y propifenazona , aminofenazona . De estas, la dipirona es quizás la más utilizada. [3] [5] Edaravonees útil para la prevención y / o terapia de lesiones de la pared arterial. [6] Eltrombopag se usa para tratar el recuento bajo de plaquetas en sangre.
Tintes [ editar ]
Los grupos pirazolona están presentes en varios colorantes importantes. Se usan comúnmente en combinación con grupos azo para dar una subfamilia de colorantes azo; a veces denominadas azopirazolonas ( tartrazina , naranja B , rojo mordiente 19 , amarillo 2G ). Acid Yellow 17 , Acid Yellow 23 (tartrazina), Pigment Yellow 13 y Pigment Red 38 se producen anualmente en una escala de varias toneladas. [1]
Ligandos [ editar ]
Se han estudiado las pirazolonas como ligandos. [7]
Referencias [ editar ]
- ↑ a b Kornis, Gabe I. (2000). "Pirazoles, pirazolinas y pirazolonas". Enciclopedia Kirk-Othmer de tecnología química . doi : 10.1002 / 0471238961.1625180111151814.a01 . ISBN 0471238961.
- ^ Knorr, Ludwig (julio de 1883). "Einwirkung von Acetessigester auf Phenylhydrazin" . Berichte der Deutschen Chemischen Gesellschaft (en alemán). 16 (2): 2597-2599. doi : 10.1002 / cber.188301602194 .
- ↑ a b Brogden, Rex N. (1986). "Derivados de pirazolona". Drogas . 32 (Suplemento 4): 60–70. doi : 10.2165 / 00003495-198600324-00006 . PMID 3552586 . S2CID 2761563 .
- ^ Brune, Kay (diciembre de 1997). "La historia temprana de los analgésicos no opioides". Dolor agudo . 1 (1): 33–40. doi : 10.1016 / S1366-0071 (97) 80033-2 .
- ^ Zhao, Zefeng; Dai, Xufen; Li, Chenyang; Wang, Xiao; Tian, Jiale; Feng, Ying; Xie, Jing; Ma, Cong; Nie, Zhuang; Fan, Peinan; Qian, Mingcheng; Él, Xirui; Wu, modelado; Zhang, Yongmin; Zheng, Xiaohui (2020). "Motivo estructural de pirazolona en química médica: retrospectiva y perspectiva" . Revista europea de química medicinal . 186 : 111893. doi : 10.1016 / j.ejmech.2019.111893 . PMC 7115706 . PMID 31761383 .
- ^ Bailly, Christian; Hecquet, Paul-Emile; Kouach, Mostafa; Thuru, Xavier; Goossens, Jean-François (2020). "Reactividad química y usos de 1-fenil-3-metil-5-pirazolona (PMP), también conocida como edaravona". Química bioorgánica y medicinal . 28 (10): 115463. doi : 10.1016 / j.bmc.2020.115463 . PMID 32241621 .
- ^ CASAS, J; GARCIATASENDE, M; SANCHEZ, A; SORDO, J; TOUCEDA, A (junio de 2007). "Modos de coordinación de 5-pirazolonas: una descripción de estado sólido". Revisiones de química de coordinación . 251 (11-12): 1561-1589. doi : 10.1016 / j.ccr.2007.02.010 .
Enlaces externos [ editar ]
- Pirazolonas en los encabezados de temas médicos (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .
- Pubchem - 3-pirazolona
- Pubchem - 4-pirazolona