Remodelación ventricular
En cardiología , la remodelación ventricular (o remodelación cardíaca ) [1] se refiere a cambios en el tamaño, la forma, la estructura y la función del corazón . Esto puede suceder como resultado del ejercicio (remodelación fisiológica) o después de una lesión en el músculo cardíaco (remodelación patológica). [2] La lesión se debe típicamente a un infarto agudo de miocardio (generalmente infarto transmural o con elevación del segmento ST), pero puede deberse a varias causas que provocan un aumento de la presión o el volumen , lo que provoca una sobrecarga de presión o una sobrecarga de volumen.(formas de tensión) en el corazón. La hipertensión crónica , la cardiopatía congénita con derivación intracardíaca y la valvulopatía cardíaca también pueden provocar remodelación. Después de que ocurre la agresión, se producen una serie de cambios histopatológicos y estructurales en el miocardio del ventrículo izquierdo que conducen a una disminución progresiva del rendimiento del ventrículo izquierdo. En última instancia, la remodelación ventricular puede resultar en una función contráctil ( sistólica ) disminuida y un volumen sistólico reducido .
La remodelación fisiológica es reversible, mientras que la remodelación patológica es en su mayoría irreversible. La remodelación de los ventrículos bajo demanda de presión izquierda / derecha hace que los desajustes sean inevitables. Los desajustes patológicos de presión entre la circulación pulmonar y sistémica guían la remodelación compensatoria de los ventrículos izquierdo y derecho. El término "remodelado inverso" en cardiología implica una mejora en la mecánica y función ventricular después de una lesión remota o un proceso patológico. [3] [4] [5]
La remodelación ventricular puede incluir hipertrofia ventricular , dilatación ventricular , cardiomegalia y otros cambios. Es un aspecto de la miocardiopatía , de las cuales existen muchos tipos. La hipertrofia concéntrica se debe a una sobrecarga de presión , mientras que la hipertrofia excéntrica se debe a una sobrecarga de volumen . [6]
El miocito cardíaco es la célula principal involucrada en la remodelación. También intervienen los fibroblastos , el colágeno , el intersticio y, en menor medida, los vasos coronarios . Un escenario común de remodelación es después de un infarto de miocardio. Hay necrosis miocárdica (muerte celular) y adelgazamiento desproporcionado del corazón. Esta área delgada y debilitada no puede soportar la presión y la carga de volumen en el corazón de la misma manera que el otro tejido sano. Como resultado, hay una dilatación de la cámara que surge de la región del infarto. La fase de remodelación inicial después de un infarto de miocardio da como resultado la reparación del área necrótica y la cicatrización del miocardio.eso puede, hasta cierto punto, considerarse beneficioso ya que hay una mejora o mantenimiento de la función del VI y del gasto cardíaco . Sin embargo, con el tiempo, a medida que el corazón experimenta una remodelación continua, se vuelve menos elíptico y más esférico. Aumento de masa y volumen ventricular, que en conjunto afectan negativamente la función cardíaca. Con el tiempo, la función diastólica o la capacidad del corazón para relajarse entre las contracciones pueden deteriorarse y provocar un deterioro adicional. [7]
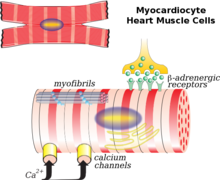
Después de un infarto de miocardio (MI), la muerte de los miocitos cardíacos puede desencadenarse por necrosis , apoptosis o autofagia , lo que lleva al adelgazamiento de la pared cardíaca. [8] Los miocitos cardíacos supervivientes se organizan en paralelo o en serie entre sí, lo que contribuye a la dilatación ventricular o la hipertrofia ventricular, según el esfuerzo de carga sobre la pared ventricular. [7] Además, también se cree que la expresión reducida de la miosina V1 y los canales de calcio de tipo L en los miocitos cardíacos causan remodelación cardíaca. En condiciones corporales normales, los ácidos grasosrepresenta del 60 al 90% del suministro de energía del corazón. Después de un infarto de miocardio, a medida que disminuye la oxidación de los ácidos grasos, se reduce el suministro de energía para los miocitos cardíacos, la acumulación de ácidos grasos a niveles tóxicos y la disfunción de las mitocondrias . Estas consecuencias también llevaron al aumento del estrés oxidativo en el corazón, provocando la proliferación de fibroblastos , activación de metaloproteinasas e inducción de apoptosis, que se explicará a continuación. Además, la respuesta inmunitaria inflamatoria después de un infarto de miocardio también contribuye a los cambios anteriores. [8]