 | |
| Datos clinicos | |
|---|---|
| Nombres comerciales | Midamor, otros |
| Otros nombres | MK-870 |
| AHFS / Drugs.com | Monografía |
Categoría de embarazo |
|
| Vías de administración | oral |
| Código ATC | |
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Biodisponibilidad | Se absorbe fácilmente, 15-25% |
| Enlace proteico | ~ 23% |
| Metabolismo | Nulo |
| Inicio de acción | 2 horas (pico a las 6-10 horas, duración ~ 24 horas) |
| Vida media de eliminación | 6 a 9 horas |
| Excreción | orina (20-50%), heces (40%) |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEBI | |
| CHEMBL | |
| Tablero CompTox ( EPA ) | |
| Tarjeta de información ECHA | 100.018.205 |
| Datos químicos y físicos | |
| Fórmula | C 6 H 8 Cl N 7 O |
| Masa molar | 229,63 g · mol −1 |
| Modelo 3D ( JSmol ) |
|
| Punto de fusion | 240,5 a 241,5 ° C (464,9 a 466,7 ° F) |
Sonrisas
| |
InChI
| |
| (verificar) | |
La amilorida , que se vende bajo el nombre comercial Midamor entre otros, es un medicamento que se usa típicamente con otros medicamentos para tratar la presión arterial alta o la hinchazón debido a insuficiencia cardíaca o cirrosis del hígado . [1] [2] La amilorida se clasifica como un diurético ahorrador de potasio. La amilorida se usa a menudo junto con otro diurético, como una tiazida o un diurético de asa . [2] Se toma por vía oral. [1] El inicio de acción es de aproximadamente dos horas y dura aproximadamente un día. [2]
Los efectos secundarios comunes incluyen niveles altos de potasio en sangre , vómitos , pérdida de apetito, sarpullido y dolor de cabeza. [1] El riesgo de niveles altos de potasio en sangre es mayor en personas con problemas renales , diabetes y personas mayores. [1] La amilorida pertenece a la familia de medicamentos diuréticos ahorradores de potasio . [1] Actúa aumentando la cantidad de sodio y disminuyendo la cantidad de potasio liberada por el túbulo distal del riñón. [2]
La amilorida fue desarrollada en 1967. [3] Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud, los medicamentos más seguros y efectivos necesarios en un sistema de salud . [4]
Usos médicos [ editar ]
La amilorida puede usarse en combinación con un diurético tiazídico para el tratamiento de la presión arterial alta o (con menos frecuencia) en combinación con un diurético de asa para el tratamiento de la insuficiencia cardíaca . Los efectos ahorradores de potasio de la amilorida compensan el bajo nivel de potasio en sangre (hipopotasemia) que a menudo es inducido por las tiazidas o los diuréticos del asa, lo cual es de particular importancia en las personas para las que mantener un nivel normal de potasio es de vital importancia. [5] Por ejemplo, las personas que toman Digitalis (es decir, digoxina ) tienen un mayor riesgo de sufrir cambios en el ritmo cardíaco si sus niveles de potasio aumentan demasiado. [5] Las guías de práctica clínica de 2017 de laEl grupo de trabajo del American College of Cardiology / American Heart Association sobre las guías de práctica clínica enumera la amilorida como un antihipertensivo oral "secundario", con una eficacia mínima. [6] Para las personas con hipertensión resistente, que ya tomaban un diurético tiazídico, un inhibidor de la enzima convertidora de angiotensina (ECA-i) o un bloqueador del receptor de angiotensina II (BRA), y un bloqueador de los canales de calcio , la adición de amilorida (o espironolactona ) fue mejor para reducir la presión arterial que agregar un bloqueador beta ( bisoprolol ) o un bloqueador alfa-1 ( doxazosina ). [7]Cuando se combinó con hidroclorotiazida, la adición de amilorida tuvo efectos positivos sobre la presión arterial y la tolerancia al azúcar en sangre. [8] Por lo tanto, la amilorida puede ser útil para prevenir los efectos secundarios metabólicos de los diuréticos tiazídicos, lo que permite el uso de dosis más altas de tiazidas (de acuerdo con la forma en que se estudiaron originalmente). [9]
La amilorida es el tratamiento de elección para el fenotipo Liddle , [10] que se caracteriza por presión arterial alta, potasio sanguíneo bajo y alcalosis metabólica junto con una actividad de renina plasmática baja y una aldosterona baja. Algunas personas con el fenotipo de Liddle tienen el síndrome de Liddle , que implica una mutación genética que produce una regulación positiva del canal de sodio epitelial (ENaC), ubicado en la membrana apical de las células epiteliales polarizadas en el túbulo distal tardío y el conducto colector del riñón. [11] Debido a que el fenotipo de Liddle generalmente implica una regulación al alza de los canales ENaC, lo que conduce a la retención de sodio y agua y a la hipopotasemia, la amilorida es útil como inhibidor de los canales ENaC debido a supromoción de la excreción de sodio y sus efectos ahorradores de potasio, restaurando el potasio a niveles normales. [12]
La amilorida se puede utilizar como monoterapia (terapia con un solo fármaco) o como terapia complementaria junto con otros diuréticos (por ejemplo , hidroclorotiazida , furosemida ) para el tratamiento de la ascitis y el edema (hinchazón) debido a la cirrosis del hígado . [5] Las guías de práctica clínica de 2012 de la Asociación Estadounidense para el Estudio de Enfermedades Hepáticas (AASLD) establecen que la amilorida se puede usar para tratar la ascitis en lugar de la espironolactona si no se tolera (p. Ej., Debido al efecto secundario de la ginecomastia ) , aunque la amilorida no es un fármaco preferido debido al costo y la falta de eficacia. [13]
Poblaciones específicas [ editar ]
Diabéticos [ editar ]
Las personas con diabetes tienen un mayor riesgo de problemas renales , lo que aumenta el riesgo de hiperpotasemia (niveles altos de potasio en sangre). El uso de amilorida en personas con diabetes requiere un control cuidadoso de la función renal y del potasio para prevenir la toxicidad. La amilorida debe suspenderse durante al menos 3 días antes de la prueba de tolerancia a la glucosa, debido al riesgo de hiperpotasemia mortal. [5]
Mala función renal [ editar ]
Las personas con función renal deficiente (p. Ej., Nitrógeno ureico en sangre > 30 mg / dL o creatinina sérica > 1,5 mg / dL) tienen un alto riesgo de hiperpotasemia. [5]
Lactancia [ editar ]
No hay datos sobre el uso de amilorida en mujeres que están amamantando. Si bien los diuréticos pueden dificultar la lactancia, es poco probable que la amilorida induzca este efecto en ausencia de otros diuréticos. [14]
Embarazo [ editar ]
Los datos del uso de amilorida en animales sugieren que no representa un riesgo para el feto en desarrollo. Sin embargo, cuando se usa en combinación con el fármaco acetazolamida durante el proceso de formación de órganos , la amilorida aumenta el riesgo de anomalías en los riñones y los uréteres. Los datos limitados en humanos sobre el uso durante el embarazo sugieren una asociación con una anomalía congénita específica del pene si se toma durante el primer trimestre, así como un riesgo de restricción leve del crecimiento intrauterino si se toma durante el embarazo. [15]
Contraindicaciones [ editar ]
La amilorida está contraindicada en personas con problemas renales (p. Ej., Anuria, enfermedad renal aguda o crónica o nefropatía diabética ), niveles elevados de potasio en sangre (≥5,5 mEq / L) o personas hipersensibles a la amilorida o cualquier ingrediente de la formulación específica. El uso también está contraindicado en personas que ya estén tomando medicamentos ahorradores de potasio (por ejemplo, espironolactona y triamtereno ) o que estén tomando suplementos de potasio (por ejemplo, cloruro de potasio) en la mayoría de las circunstancias. [1]
Efectos adversos [ editar ]
En general, la amilorida se tolera bien. [16] Los efectos adversos comunes del uso de amilorida incluyen niveles elevados de potasio en sangre, erupciones cutáneas leves, dolores de cabeza y efectos secundarios gastrointestinales (náuseas, vómitos, diarrea, disminución del apetito , flatulencia y dolor abdominal). [1] Los síntomas leves de concentraciones altas de potasio en sangre incluyen sensaciones cutáneas inusuales , debilidad muscular o fatiga, pero pueden presentarse síntomas más graves como parálisis flácida de las extremidades, frecuencia cardíaca lenta e incluso shock . [1]
Sobredosis [ editar ]
No existen datos de sobredosis de amilorida en humanos, aunque se espera que una sobredosis produzca efectos consistentes con sus efectos terapéuticos; por ejemplo, deshidratación por exceso de diuresis y alteraciones electrolíticas relacionadas con la hiperpotasemia. Se desconoce si la amilorida se puede dializar y no existe un antídoto específico contra ella. El tratamiento generalmente es de apoyo, aunque se puede tratar la hiperpotasemia. [dieciséis]
Interacciones [ editar ]
La amilorida puede tener interacciones medicamentosas importantes cuando se combina con otros medicamentos que también aumentan los niveles de potasio en la sangre, lo que produce hiperpotasemia. [17] Por ejemplo, la combinación de amilorida con inhibidores de la enzima convertidora de angiotensina (ECA) como lisinopril , o antagonistas del receptor de angiotensina II tipo 1 (AT 1 ) como losartán , puede producir niveles altos de potasio en la sangre, lo que requiere un control frecuente . [17]
Farmacología [ editar ]
Mecanismo de acción [ editar ]
Diuresis [ editar ]
La amilorida actúa bloqueando directamente el canal de sodio epitelial (ENaC) con un IC 50 alrededor de 0,1 M , lo que indica potente bloqueo. [18] El antagonismo de ENaC inhibe así la reabsorción de sodio en los túbulos contorneados distales tardíos , los túbulos de conexión y los conductos colectores en la nefrona . [19] Esto promueve la pérdida de sodio y agua del cuerpo y reduce la excreción de potasio . El medicamento se usa a menudo junto con un diurético tiazídico para contrarrestar el efecto de pérdida de potasio. Debido a sus capacidades ahorradoras de potasio, la hiperpotasemia(concentración elevada de potasio en la sangre). El riesgo de desarrollar hiperpotasemia aumenta en pacientes que también toman inhibidores de la ECA , antagonistas del receptor de angiotensina II , otros diuréticos ahorradores de potasio o cualquier suplemento que contenga potasio.
Varios [ editar ]
Una fracción de los efectos de la amilorida es la inhibición de los canales catiónicos cíclicos activados por GMP en el conducto colector medular interno . [20]
La amilorida tiene una segunda acción sobre el corazón, bloqueando los intercambiadores de sodio-hidrógeno antiportador 1 o NHE-1 de Na + / H + . Esto minimiza la lesión por reperfusión en los ataques isquémicos. [ cita requerida ]
La amilorida también bloquea el antiportador Na + / H + en la superficie apical de las células del túbulo proximal en la nefrona, eliminando más del 80% de la acción de la angiotensina II sobre la secreción de iones de hidrógeno en las células del túbulo proximal. [21] Tenga en cuenta que la amilorida no es un bloqueador del receptor de angiotensina II (como losartán , por ejemplo). El transportador de Na-H también se encuentra en el yeyuno del intestino delgado, como resultado, la amilorida también bloquea la reabsorción de Na y, por lo tanto, de agua en los intestinos. [22]
Se considera que la amilorida es un inhibidor reversible del canal iónico sensible al panácido (ASIC) que evita el flujo transitorio de iones pero no el flujo sostenido de iones. Los ASIC son miembros de la familia de canales de proteínas ENaC y se encuentran en el sistema nervioso , el sistema cardiovascular , el sistema gastrointestinal y la piel . En términos generales, los ASIC participan en la detección de daños , la quimiosensación (cambios de pH específicamente) y el tacto . [23]
Farmacocinética [ editar ]
Absorción [ editar ]
La amilorida tiene una biodisponibilidad oral del 50%, lo que significa que aproximadamente el 50% de una dosis oral se absorbe en el torrente sanguíneo. La coadministración con alimentos reduce la cantidad de amilorida que es absorbida por el cuerpo en aproximadamente un 30%, aunque no afecta la tasa de absorción. Sin embargo, tomar amilorida con alimentos ayuda a reducir la incidencia de sus efectos secundarios gastrointestinales. Después de tomarla, el efecto diurético de la amilorida ocurre dentro de las 2 horas, con un pico de diuresis dentro de las 6 a 10 horas. Los efectos diuréticos de la amilorida persisten durante aproximadamente 24 horas después de la administración. [1]
Distribución [ editar ]
La amilorida atraviesa la placenta y se distribuye en la leche materna in vivo . [1]
Metabolismo [ editar ]
La amilorida no es metabolizada por el hígado . [1] En comparación, el triamtereno, un inhibidor de ENaC, es metabolizado por el hígado. [24]
Excreción [ editar ]
Aproximadamente el 50% de la amilorida se excreta sin cambios por los riñones, mientras que alrededor del 40% se excreta en las heces (probablemente fármaco que no se absorbió). La vida media de la amilorida en humanos es de entre 6 y 9 horas, que puede prolongarse en personas con función renal deficiente. [1]
Farmacogenómica [ editar ]
Un polimorfismo de un solo nucleótido (SNP) en la proteína NEDD4L puede afectar la forma en que la amilorida afecta la presión arterial de una persona en personas con presión arterial alta . [25]
Química [ editar ]
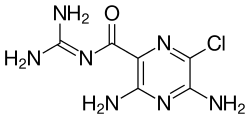
La estructura química de la amilorida se compone de una estructura de anillo de pirazina sustituida con un sustituyente de carbonilguanidinio. [26] El pKa de la amilorida es 8,67, que se debe al grupo guanidinio . [26] En ambientes de pH alto (alcalino, baja concentración de hidrógeno ), el grupo guanidinio se desprotona y el compuesto se vuelve neutro, lo que agota su actividad en los canales de sodio. [26] La amilorida, como sustancia pura, es altamente fluorescente , con longitudes de onda de excitación a 215, 288 y 360 nm, y emite luz a 420 nm. [27]
Historia [ editar ]
La amilorida fue sintetizada y descubierta por primera vez por los laboratorios de investigación Merck Sharp y Dohme a fines de la década de 1960. [26] El fármaco fue descubierto como parte de un proceso de selección de sustancias químicas que revirtieron los efectos de los mineralocorticoides in vivo . [26] La amilorida fue el único fármaco en la pantalla que fue capaz de causar la excreción de sodio (natriuresis) sin una excreción urinaria concomitante de potasio (kaliuresis). [26] Se han estudiado miles de análogos de amilorida desde su descubrimiento inicial, que se han utilizado para estudiar los efectos de los transportadores de sodio. [26]
La amilorida fue aprobada por la Administración de Drogas y Alimentos de los Estados Unidos (FDA) el 5 de octubre de 1981. [28]
Sociedad y cultura [ editar ]
Está en la Lista de medicamentos esenciales de la Organización Mundial de la Salud . [4]
Amiloride está en la lista de sustancias prohibidas de la Agencia Mundial Antidopaje , ya que se considera un agente enmascarante . [29] Los diuréticos como la amilorida actúan como agentes enmascaradores al reducir la concentración de otros agentes dopantes debido a que promueven la diuresis, aumentando el volumen total de la orina. [24] La lista incluye otros diuréticos ahorradores de potasio, como el triamtereno y la espironolactona . [29] En 2008, se encontraron amilorida y el diurético triamtereno ahorrador de potasio en el 3% de las muestras positivas de dopaje diurético. [24]
Formulaciones y nombres comerciales [ editar ]
- Clorhidrato de amilorida
- Midamor (Estados Unidos)
- Co-amilozida (clorhidrato de amilorida con hidroclorotiazida )
- Co-amilofrusa (clorhidrato de amilorida con furosemida )
- Clorhidrato de amilorida con ciclopentiazida
- Clorhidrato de amilorida con bumetanida
Investigación [ editar ]
La amilorida es un inhibidor de NHE-1, que ayuda a mantener el pH normal dentro de las células. Las células cancerosas en la leucemia , un tipo de cáncer de la sangre, tienen un pH más alto en comparación con las células normales. La amilorida afecta el empalme y la regulación de múltiples genes involucrados en el cáncer, aunque no parecen estar directamente relacionados con sus efectos sobre el pH. La amilorida se ha probado in vitro como un complemento del fármaco anticanceroso imatinib , que parece mostrar un efecto sinérgico. Versiones modificadas de amilorida, conocida como 5 '- (N, N-dimetil) -amilorida (DMA), 5-N-etil-N-isopropilamilorida (EIPA) y 5- (N, N-hexametileno) -amilorida ( HMA), se están estudiando para el tratamiento de la leucemia . [30]
La fibrosis quística es un trastorno genético debido a una mutación en el gen CFTR , que codifica el canal de cloruro CFTR. [18] Existe evidencia que sugiere que el objetivo molecular de la amilorida, ENaC, también está implicado en la fibrosis quística debido a sus efectos sobre la mucosidad en los pulmones. [18] Las formulaciones de amilorida en aerosol se han probado en ensayos clínicos, aunque los ensayos clínicos a largo plazo no han demostrado mucha utilidad. [18] Debido a su corta duración de acción, se pensó que los inhibidores de ENaC de acción más prolongada podrían resultar más efectivos. [31] Sin embargo, los inhibidores de ENaC de acción prolongada (es decir, benzamil) también han fallado los ensayos clínicos, a pesar de una mejora tanto en la solubilidad como en la potencia de los fármacos. [18] Un análogo de amilorida de tercera generación (metanosulfonato de N- (3,5-diamino-6-cloropirazina-2-carbonil) -N'-4- [4- (2,3-dihidroxipropoxi) fenil] butil-guanidina, [ 32] nombre de la investigación "552-02"), con mejores propiedades farmacocinéticas , se está estudiando. [18]
El dolor inducido por la exposición al ácido se atenúa con amilorida en ensayos en humanos, lo que puede indicar un papel de la amilorida en el tratamiento del dolor en el futuro. [18]
Referencias [ editar ]
- ^ a b c d e f g h i j k l "Clorhidrato de amilorida" . La Sociedad Estadounidense de Farmacéuticos del Sistema de Salud. Archivado desde el original el 27 de diciembre de 2016 . Consultado el 8 de diciembre de 2016 .
- ^ a b c d Organización Mundial de la Salud (2009). Stuart MC, Kouimtzi M, Hill SR (eds.). Formulario modelo de la OMS 2008 . Organización Mundial de la Salud. págs. 328, 330. hdl : 10665/44053 . ISBN 9789241547659.
- ^ Progresos en la investigación de medicamentos / Fortschritte der Arzneimittelforschung / Progrés des recherches pharmaceutiques . Birkhäuser. 2013. p. 210. ISBN 9783034870948. Archivado desde el original el 28 de diciembre de 2016.
- ^ a b Organización Mundial de la Salud (2019). Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud: 21a lista 2019 . Ginebra: Organización Mundial de la Salud. hdl : 10665/325771 . WHO / MVP / EMP / IAU / 2019.06. Licencia: CC BY-NC-SA 3.0 IGO.
- ^ a b c d e "Monografía del producto MIDAMOR" (PDF) . AA Pharma Inc. 25 de agosto de 2010 . Consultado el 7 de junio de 2018 .
- ^ Whelton PK, Carey RM, Aronow WS, Casey DE, Collins KJ, Dennison Himmelfarb C, et al. (Junio de 2018). "2017 ACC / AHA / AAPA / ABC / ACPM / AGS / APhA / ASH / ASPC / NMA / PCNA Directriz para la prevención, detección, evaluación y manejo de la presión arterial alta en adultos: un informe del Colegio Americano de Cardiología / Grupo de trabajo de la Asociación Americana del Corazón sobre guías de práctica clínica " . La hipertensión . 71 (6): e13 – e115. doi : 10.1161 / HYP.0000000000000065 . PMID 29133356 .
- ^ Williams B, MacDonald TM, Morant SV, Webb DJ, Sever P, McInnes GT, et al. (Junio de 2018). "Cambios endocrinos y hemodinámicos en la hipertensión resistente y respuestas de la presión arterial a la espironolactona o amilorida: los subestudios de los mecanismos PATHWAY-2" . La lanceta. Diabetes y endocrinología . 6 (6): 464–475. doi : 10.1016 / S2213-8587 (18) 30071-8 . PMC 5966620 . PMID 29655877 .
- ^ Bavry A. "Prevención y tratamiento de la hipertensión con algoritmo basado therapyY-3 - American College of Cardiology" . Colegio Americano de Cardiología . Fundación del Colegio Americano de Cardiología . Consultado el 9 de junio de 2018 .
- ^ O'Riordan M. "PATHWAY3: Amiloride-HCTZ reduce BP con efecto neutral sobre glucosa, potasio" . www.medscape.com . WebMD LLC . Consultado el 9 de junio de 2018 .
- ^ Spence JD (mayo de 2017). "La terapia médica racional es la clave para una prevención eficaz de las enfermedades cardiovasculares". La Revista Canadiense de Cardiología . 33 (5): 626–634. doi : 10.1016 / j.cjca.2017.01.003 . PMID 28449833 .
- ^ Kellenberger S, Schild L (2015). "Unión Internacional de Farmacología Básica y Clínica. XCI. Estructura, función y farmacología de los canales iónicos sensibles al ácido y el canal epitelial de Na +" . Revisiones farmacológicas . 67 (1): 1–35. doi : 10.1124 / pr.114.009225 . PMID 25287517 .
- ^ Tetti M, Monticone S, Burrello J, Matarazzo P, Veglio F, Pasini B, et al. (Marzo de 2018). "Síndrome de Liddle: revisión de la literatura y descripción de un nuevo caso" . Revista Internacional de Ciencias Moleculares . 19 (3): 812. doi : 10.3390 / ijms19030812 . PMC 5877673 . PMID 29534496 .
- ^ Runyon B (2012). "Manejo de pacientes adultos con ascitis debida a cirrosis: actualización de 2012" (PDF) . Asociación Estadounidense para el Estudio de la Enfermedad Hepática. Archivado desde el original (PDF) el 12 de junio de 2018 . Consultado el 8 de junio de 2018 .
- ^ "LACTMED: AMILORIDE" . TOXNET . Biblioteca Nacional de Medicina de EE. UU . Consultado el 7 de junio de 2018 .
- ^ "Búsqueda de drogas SafeFetus" . SafeFetus.com . SafeFetus.com. Archivado desde el original el 12 de junio de 2018 . Consultado el 8 de junio de 2018 .
- ^ a b "Paquete de aprobación para NDA 18-200 / S-024". Centro de Evaluación e Investigación de Medicamentos. Falta o vacío
|url=( ayuda ) - ^ a b "Medicamentos e hiperpotasemia" . Medsafe . Ministerio de Salud de Nueva Zelanda . Consultado el 13 de abril de 2019 .
- ↑ a b c d e f g Qadri YJ, Rooj AK, Fuller CM (abril de 2012). "ENaCs y ASICs como dianas terapéuticas" . Revista estadounidense de fisiología. Fisiología celular . 302 (7): C943-65. doi : 10.1152 / ajpcell.00019.2012 . PMC 3330738 . PMID 22277752 .
- ^ Loffing J, Kaissling B (abril de 2003). "Vías de transporte de sodio y calcio a lo largo de la nefrona distal de los mamíferos: de conejo a ser humano". Revista estadounidense de fisiología. Fisiología renal . 284 (4): F628-43. doi : 10.1152 / ajprenal.00217.2002 . PMID 12620920 .
- ^ Walter F. Boron (2005). Fisiología médica: un enfoque celular y molecular . Elsevier / Saunders. ISBN 978-1-4160-2328-9. página 875
- ^ Cogan MG (mayo de 1990). "Angiotensina II: un potente controlador del transporte de sodio en el túbulo proximal temprano" . La hipertensión . 15 (5): 451–8. doi : 10.1161 / 01.HYP.15.5.451 . PMID 2185149 . Archivado desde el original el 19 de septiembre de 2016.
- ^ Gurney MA, Laubitz D, Ghishan FK, Kiela PR (enero de 2017). "+ intercambio" . Gastroenterología y Hepatología Celular y Molecular . 3 (1): 27–40. doi : 10.1016 / j.jcmgh.2016.09.010 . PMC 5235326 . PMID 28090568 .
- ^ Cheng YR, Jiang BY, Chen CC (mayo de 2018). "Canales iónicos de detección de ácido: proteínas de doble función para la detección de quimio y la detección de mecano" . Revista de Ciencias Biomédicas . 25 (1): 46. doi : 10.1186 / s12929-018-0448-y . PMC 5966886 . PMID 29793480 .
- ↑ a b c Cadwallader AB, de la Torre X, Tieri A, Botrè F (septiembre de 2010). "El abuso de diuréticos como fármacos potenciadores del rendimiento y agentes enmascaradores en el dopaje deportivo: farmacología, toxicología y análisis" . Revista británica de farmacología . 161 (1): 1–16. doi : 10.1111 / j.1476-5381.2010.00789.x . PMC 2962812 . PMID 20718736 .
- ^ "Amilorida - Anotación de variante" . PharmGKB . PharmGKB . Consultado el 8 de junio de 2018 .
- ↑ a b c d e f g Palmer LG, Kleyman TR (1995). "Diuréticos que retienen potasio: amilorida". En Greger RF, Knauf H, Mutschler E (eds.). Diuréticos . Berlín, Heidelberg: Springer Berlin Heidelberg. págs. 363–394. ISBN 978-3-642-79565-7.
- ^ Sunkara P, ed. (2017). "11. Quimioterapia contra el cáncer y el flujo de sodio". Enfoques novedosos para la quimioterapia contra el cáncer . Elsevier. pag. 363. ISBN 9781483272177.
- ^ "amilorida" . drugcentral.org . División de Informática Traslacional de la Universidad de Nuevo México . Consultado el 8 de junio de 2018 .
- ^ a b "S5. Diuréticos y agentes enmascaradores - WADA" . Agencia Mundial Antidopaje . Enero de 2016. Archivado desde el original el 27 de septiembre de 2016 . Consultado el 1 de septiembre de 2016 .
- ^ Mihaila RG (diciembre de 2015). "Un minireview sobre los inhibidores de NHE1. Una esperanza redescubierta en oncohematología" . Artículos biomédicos de la Facultad de Medicina de la Universidad Palacky, Olomouc, Checoslovaquia . 159 (4): 519–26. doi : 10.5507 / bp.2015.060 . PMID 26725705 .
- ^ Rodgers HC, Knox AJ (junio de 2001). "Tratamiento farmacológico del defecto bioquímico en las vías respiratorias de la fibrosis quística" . The European Respiratory Journal . 17 (6): 1314–21. doi : 10.1183 / 09031936.01.00086201 . PMID 11491179 .
- ^ Hirsh AJ, Zhang J, Zamurs A, Fleegle J, Thelin WR, Caldwell RA, et al. (Abril de 2008). "Propiedades farmacológicas del metanosulfonato de N- (3,5-diamino-6-cloropirazina-2-carbonil) -N'-4- [4- (2,3-dihidroxipropoxi) fenil] butil-guanidina (552-02), un nuevo bloqueador de los canales de sodio epitelial con potencial eficacia clínica para la enfermedad pulmonar por fibrosis quística ". La Revista de Farmacología y Terapéutica Experimental . 325 (1): 77–88. doi : 10.1124 / jpet.107.130443 . PMID 18218832 . S2CID 40732094 .
Enlaces externos [ editar ]
- "Amilorida" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.