 | |
 | |
| Datos clinicos | |
|---|---|
| Nombres comerciales | Lunesta, Eszop, otros |
| AHFS / Drugs.com | Monografía |
| MedlinePlus | a605009 |
| Datos de licencia |
|
| Vías de administración | Por vía oral ( tabletas ) |
| Código ATC | |
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Enlace proteico | 52–59% |
| Metabolismo | Oxidación y desmetilación del hígado ( mediadas por CYP3A4 y CYP2E1 ) |
| Vida media de eliminación | 6 horas |
| Excreción | Riñón |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII |
|
| KEGG |
|
| CHEBI |
|
| CHEMBL |
|
| Tablero CompTox ( EPA ) |
|
| Tarjeta de información ECHA | 100.149.304 |
| Datos químicos y físicos | |
| Fórmula | C 17 H 17 Cl N 6 O 3 |
| Masa molar | 388,81 g · mol −1 |
| Modelo 3D ( JSmol ) |
|
Sonrisas
| |
InChI
| |
| (verificar) | |
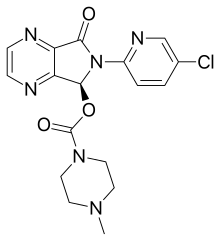
La eszopiclona , vendida bajo la marca Lunesta entre otros, es un medicamento que se usa en el tratamiento del insomnio . [2] La evidencia respalda un beneficio leve a moderado hasta seis meses. [3] [2] [4] Se toma por vía oral. [3]
Los efectos secundarios comunes incluyen dolor de cabeza, sequedad de boca , náuseas y mareos. [3] Los efectos secundarios graves pueden incluir pensamientos suicidas , abuso, alucinaciones y angioedema . [3] Se recomienda un mayor cuidado en personas con problemas hepáticos y personas mayores. [3] La disminución rápida de la dosis puede provocar la abstinencia. [3] La eszopiclona se clasifica como un hipnótico sedante no benzodiazepínico y como una ciclopirrolona . [5] Es el estereoisómero S de zopiclona . [3]Funciona al interactuar con los receptores GABA . [5]
Aprobada para uso médico en los Estados Unidos en 2004, la eszopiclona está disponible como medicamento genérico . [3] En 2017, fue el medicamento 214 más recetado en los Estados Unidos, con más de dos millones de recetas. [6] [7] La eszopiclona no se vende en la Unión Europea , ya que en 2009 la EMA dictaminó que era demasiado similar a la zopiclona para ser considerada un nuevo producto patentable. [8] [9]
Usos médicos [ editar ]
Una revisión Cochrane de 2018 encontró que produjo una mejora moderada en el inicio y el mantenimiento del sueño. Los autores sugieren que cuando se han agotado las estrategias de tratamiento no farmacológicas preferidas, la eszopiclona proporciona un tratamiento eficaz para el insomnio. [10] En 2014, la USFDA pidió que la dosis inicial se redujera de 2 miligramos a 1 miligramo después de que se observó en un estudio que incluso 8 horas después de tomar el medicamento por la noche, algunas personas no podían hacer frente a su siguiente actividades diurnas como conducir y otras actividades que requieren un estado de alerta total. [11]
La eszopiclona es ligeramente eficaz en el tratamiento del insomnio, donde la dificultad para conciliar el sueño es el síntoma principal. [2] Kirsch y col. encontró que el beneficio sobre el placebo tiene una importancia clínica cuestionable. [2] Aunque el efecto del fármaco y la respuesta al placebo fueron bastante pequeños y de importancia clínica cuestionable, los dos juntos producen una respuesta clínica razonablemente grande. [2] No se recomienda para uso crónico en ancianos. [12]
Anciano [ editar ]
Los fármacos hipnóticos sedantes, incluida la eszopiclona, se prescriben con más frecuencia a los ancianos que a los pacientes más jóvenes, a pesar de que los beneficios de la medicación generalmente no son impresionantes. Se debe tener cuidado al elegir un fármaco hipnótico apropiado y, si se inicia la terapia con el fármaco, se debe iniciar con la dosis más baja posible para minimizar los efectos secundarios. [13]
En 2015, la American Geriatrics Society revisó la información de seguridad sobre la eszopiclona y medicamentos similares y concluyó que los "hipnóticos agonistas del receptor de benzodiazepinas no benzodiazepínicos (eszopiclona, zaleplon , zolpidem ) deben evitarse sin considerar la duración del uso debido a su asociación con los daños equilibrado con su mínima eficacia en el tratamiento del insomnio ".
La revisión tomó esta determinación debido a los peligros relativamente grandes para las personas mayores del zolpidem y otros "medicamentos z" junto con el hecho de que los medicamentos tienen "una eficacia mínima en el tratamiento del insomnio". Este fue un cambio de la recomendación de la AGS de 2012, que sugería limitar el uso a 90 días o menos. La revisión declaró: "[se] eliminó la advertencia de uso de 90 días de los hipnóticos agonistas del receptor de benzodiazepinas no benzodiazepínicos, lo que resultó en una declaración de 'evitar' inequívoca (sin advertencias) debido al aumento en la evidencia de daño en esta área desde el Actualización de 2012 ". [14]
Una revisión extensa de la literatura médica con respecto al manejo del insomnio y los ancianos encontró que existe evidencia considerable de la efectividad y durabilidad de los tratamientos no farmacológicos para el insomnio en adultos de todas las edades y que estas intervenciones están infrautilizadas. En comparación con las benzodiazepinas, los sedantes hipnóticos no benzodiazepínicos , incluida la eszopiclona, parecían ofrecer pocas ventajas clínicas significativas, si es que tenían alguna, en cuanto a eficacia o tolerabilidad en personas de edad avanzada. Se encontró que agentes más nuevos con mecanismos de acción novedosos y perfiles de seguridad mejorados, como los agonistas del receptor de melatonina, son prometedores para el tratamiento del insomnio crónico en personas mayores. El uso a largo plazo de sedantes-hipnóticos para el insomnio carece de una base de evidencia y tradicionalmente se ha desaconsejado por razones que incluyen preocupaciones sobre los posibles efectos adversos de los medicamentos como deterioro cognitivo ( amnesia anterógrada ), sedación diurna, incoordinación motora y mayor riesgo de vehículos motorizados. accidentes y caídas. Además, queda por determinar la eficacia y seguridad del uso a largo plazo de estos agentes. Se concluyó que se necesita más investigación para evaluar los efectos a largo plazo del tratamiento y la estrategia de manejo más adecuada para las personas mayores con insomnio crónico. [15]
Un metanálisis de 2009 encontró una tasa más alta de infecciones . [dieciséis]
Efectos adversos [ editar ]
Las pastillas para dormir, incluida la eszopiclona, se han asociado con un mayor riesgo de muerte. [17]
La hipersensibilidad a la eszopiclona es una contraindicación para su uso. Algunos efectos secundarios son más comunes que otros. Las recomendaciones sobre el uso de eszopiclona pueden verse modificadas por otras condiciones de salud. Estas condiciones o circunstancias pueden ocurrir en personas que tienen un metabolismo reducido y otras condiciones. Se puede considerar la presencia de insuficiencia hepática, lactancia y actividades que requieran alerta mental (por ejemplo, conducir) al determinar la frecuencia y la dosis. [5]
- sabor desagradable [5]
- dolor de cabeza [5]
- edema periférico [5] [18]
- dolor de pecho [5]
- pensamiento anormal [5]
- cambios de comportamiento [5]
- depresión [5] [18]
- alucinaciones [5] [18]
- conducción dormida [5] y sonambulismo
- boca seca [5]
- erupción [5] [18]
- patrones de sueño alterados [5]
- coordinación deteriorada [5]
- mareos [5]
- somnolencia diurna [5]
- picazón [18]
- micción frecuente o dolorosa [18]
- dolor de espalda [18]
- comportamiento agresivo [18]
- confusión [18]
- agitación [18]
- pensamientos suicidas [18]
- despersonalización [18]
- amnesia [18]
Un metanálisis de 2009 encontró una tasa 44% más alta de infecciones leves , como faringitis o sinusitis , en personas que tomaban eszopiclona u otros fármacos hipnóticos en comparación con las que tomaban un placebo. [19]
Dependencia [ editar ]
En los Estados Unidos, la eszopiclona es una sustancia controlada de categoría IV según la Ley de Sustancias Controladas . El uso de eszopiclona puede provocar dependencia física y psicológica. [5] [20] El riesgo de abuso y dependencia aumenta con la dosis y la duración del uso y el uso concomitante de otras drogas psicoactivas. El riesgo también es mayor en pacientes con antecedentes de abuso de alcohol u otras drogas o antecedentes de trastornos psiquiátricos. Se puede desarrollar tolerancia después del uso repetido de benzodiazepinas y medicamentos similares a las benzodiazepinas durante algunas semanas.
Un estudio financiado y realizado por Sepracor no encontró signos de tolerancia o dependencia en un grupo de pacientes seguidos durante hasta seis meses. [20]
Abuso [ editar ]
Un estudio del potencial de abuso de eszopiclona encontró que en personas con antecedentes conocidos de abuso de benzodiazepinas, la eszopiclona en dosis de 6 y 12 mg producía efectos similares a los del diazepam 20 mg. El estudio encontró que en estas dosis que son dos o más veces mayores que las dosis máximas recomendadas, se observó un aumento relacionado con la dosis en los informes de amnesia, sedación, somnolencia y alucinaciones tanto para eszopiclona (Lunesta) como para diazepam ( Valium ). [18]
Sobredosis [ editar ]
De acuerdo con la información de prescripción de EE. UU., Se han informado sobredosis de eszopiclona hasta 90 veces la dosis recomendada en las que el paciente se recuperó por completo. Según la edición de mayo de 2014 de la Información de prescripción oficial de EE. UU. , Se han informado muertes solo en casos en los que la eszopiclona se combinó con otras drogas o alcohol. [21]
Los centros de control de intoxicaciones informaron que entre 2005 y 2006 se registraron un total de 525 sobredosis de eszopiclona en el estado de Texas , la mayoría de las cuales fueron intentos de suicidio intencionales . [22]
Si se consume en la última hora, la sobredosis de eszopiclona puede tratarse con la administración de carbón activado o mediante lavado gástrico . [23]
Interacciones [ editar ]
Existe un mayor riesgo de depresión del sistema nervioso central cuando se toma eszopiclona junto con otros agentes depresores del SNC, incluidos antipsicóticos , hipnóticos sedantes (como barbitúricos o benzodiazepinas), antihistamínicos , opioides , fenotiazinas y algunos antidepresivos. También existe un mayor riesgo de depresión del sistema nervioso central con otros medicamentos que inhiben las actividades metabólicas del sistema enzimático CYP3A4 del hígado . Los medicamentos que inhiben este sistema enzimático incluyen nelfinavir , ritonavir , ketoconazol ,itraconazol y claritromicina . El alcohol también tiene un efecto aditivo cuando se usa simultáneamente con eszopiclona. [5] La eszopiclona es más eficaz si no se toma después de una comida copiosa con alto contenido de grasa. [5]
Farmacología [ editar ]
La eszopiclona actúa sobre el sitio de unión de las benzodiazepinas situado en las neuronas GABA A como modulador alostérico positivo . [24] La eszopiclona se absorbe rápidamente después de la administración oral, con niveles séricos que alcanzan un pico entre 0.45 y 1.3 horas. [25] [5] La vida media de eliminación de la eszopiclona es de aproximadamente 6 horas y se metaboliza ampliamente por oxidación y desmetilación. Aproximadamente del 52% al 59% de una dosis se une débilmente a las proteínas plasmáticas. Isoenzimas CYP3A4 y CYP2E1 del citocromo P450 (CYP)están involucrados en la biotransformación de eszopiclona; por tanto, los fármacos que inducen o inhiben estas isoenzimas CYP pueden afectar el metabolismo de la eszopiclona. Menos del 10% de la dosis administrada por vía oral se excreta en la orina como zopiclona racémica. [26] En términos de unión al receptor de benzodiazepinas y potencia relevante, 3 mg de eszopiclona equivalen a 10 mg de diazepam . [27]
Historia [ editar ]
En un controvertido artículo de 2009 en el New England Journal of Medicine, "Perdido en la transmisión: información de la FDA sobre medicamentos que nunca llega a los médicos", se informó que el mayor de los tres ensayos de Lunesta encontró que, en comparación con el placebo, Lunesta "era superior al placebo", mientras que solo acortaba el tiempo inicial para quedarse dormido en 15 minutos en promedio . "Los médicos interesados en la eficacia del fármaco no pueden encontrar información sobre la eficacia en la etiqueta: solo indica que Lunesta es superior al placebo. La revisión médica de la FDA proporciona datos de eficacia, aunque no hasta la página 306 del documento de 403 páginas. , el ensayo más grande de fase 3, los pacientes del grupo Lunesta informaron que se dormían un promedio de 15 minutos más rápido y dormían un promedio de 37 minutos más que los del grupo de placebo. Sin embargo, en promedio,Los pacientes de Lunesta aún cumplían los criterios para el insomnio y no informaron ninguna mejora clínicamente significativa en el estado de alerta o el funcionamiento al día siguiente ".[28]
Disponibilidad en Europa [ editar ]
El 11 de septiembre de 2007, Sepracor firmó un acuerdo de marketing con la compañía farmacéutica británica GlaxoSmithKline por los derechos para vender eszopiclona (bajo el nombre de Lunivia en lugar de Lunesta) en Europa . [29] Se esperaba que Sepracor recibiera aproximadamente $ 155 millones si el trato se concretaba. [29] En 2008, Sepracor presentó una solicitud a la EMA (el equivalente de la Unión Europea a la FDA de EE. UU. ) Para obtener autorización para comercializar el medicamento en la UE, e inicialmente recibió una respuesta favorable. [30]Sin embargo, Sepracor retiró su solicitud de autorización en 2009 después de que la EMA declarara que no otorgaría el estatus de 'nueva sustancia activa' a la eszopiclona, ya que era esencialmente farmacológica y terapéuticamente demasiado similar a la zopiclona para ser considerada un nuevo producto patentable. [31] Dado que la patente de la zopiclona ha expirado, esta decisión habría permitido a las empresas rivales producir también legalmente versiones genéricas más baratas de eszopiclona para el mercado europeo. [32] En noviembre de 2012 [actualizar], Sepracor no ha vuelto a presentar su solicitud de autorización y la eszopiclona no está disponible en Europa. El acuerdo con GSK fracasó y GSK lanzó un acuerdo de $ 3.3 mil millones para comercializar Actelion'stableta para dormir de almorexant , que entró en ensayos médicos de fase 3 antes de que se abandonara el desarrollo debido a los efectos secundarios. [ cita requerida ]
Referencias [ editar ]
- ^ Grupo de trabajo internacional de la OMS para la metodología de estadísticas de medicamentos (27 de agosto de 2008). "Clasificación ATC / DDD (FINAL): Nuevos códigos ATC de quinto nivel" . Centro Colaborador de la OMS para la Metodología de Estadísticas de Medicamentos. Archivado desde el original el 6 de mayo de 2008 . Consultado el 5 de septiembre de 2008 .
- ^ a b c d e Huedo-Medina, TB; Kirsch, yo; Middlemass, J; Klonizakis, M; Siriwardena, AN (17 de diciembre de 2012). "Eficacia de los hipnóticos no benzodiazepínicos en el tratamiento del insomnio en adultos: metanálisis de los datos presentados a la Administración de Alimentos y Medicamentos" . BMJ (Ed. De investigación clínica) . 345 : e8343. doi : 10.1136 / bmj.e8343 . PMC 3544552 . PMID 23248080 .
- ^ a b c d e f g h "Monografía de eszopiclona para profesionales" . Drugs.com . Sociedad Estadounidense de Farmacéuticos del Sistema de Salud . Consultado el 6 de abril de 2019 .
- ^ Rösner, S; Englbrecht, C; Wehrle, R; Hajak, G; Soyka, M (10 de octubre de 2018). "Eszopiclone para el insomnio" . La base de datos Cochrane de revisiones sistemáticas . 10 : CD010703. doi : 10.1002 / 14651858.CD010703.pub2 . PMC 6492503 . PMID 30303519 .
- ^ a b c d e f g h i j k l m n o p q r s t u v "Eszopiclone" (PDF) . FA Davis. 2017 . Consultado el 15 de abril de 2017 .
- ^ "El Top 300 de 2020" . ClinCalc . Consultado el 11 de abril de 2020 .
- ^ "Eszopiclona - estadísticas de uso de drogas" . ClinCalc . Consultado el 11 de abril de 2020 .
- ^ "El fin del acuerdo de Sepracor-GSK plantea una pregunta en la lucha de patentes de Lunesta" . www.cbsnews.com . 13 de junio de 2009 . Consultado el 7 de abril de 2019 .
- ^ "Sepracor Pharmaceuticals Ltd retira su solicitud de autorización de comercialización para Lunivia (eszopiclona)" . Agencia Europea de Medicamentos . 15 de junio de 2009 . Consultado el 7 de abril de 2019 .
- ^ Rösner, Susanne; Englbrecht, Christian; Wehrle, Renate; Hajak, Göran; Soyka, Michael (10 de octubre de 2018). "Eszopiclone para el insomnio" . Base de datos Cochrane de revisiones sistemáticas . 10 : CD010703. doi : 10.1002 / 14651858.CD010703.pub2 . PMC 6492503 . PMID 30303519 .
- ^ "La FDA estadounidense reduce la dosis inicial de eszopiclona de 2 mg a 1 mg" .
- ^ Experto en actualización de criterios de cervezas de la American Geriatrics Society 2012, Panel (abril de 2012). "American Geriatrics Society actualizó los criterios de Beers para el uso de medicamentos potencialmente inapropiados en adultos mayores" . Revista de la Sociedad Americana de Geriatría . 60 (4): 616–31. doi : 10.1111 / j.1532-5415.2012.03923.x . PMC 3571677 . PMID 22376048 .
- ^ Tariq SH, Pulisetty S (febrero de 2008). "Farmacoterapia para el insomnio". Clin Geriatr Med . 24 (1): 93-105, vii. doi : 10.1016 / j.cger.2007.08.009 . PMID 18035234 .
- ^ Fick DM , Semla TP, Beizer J, Brandt N (2015). "American Geriatrics Society 2015 Criterios actualizados de Beers para el uso de medicamentos potencialmente inapropiados en adultos mayores" (PDF) . Revista de la Sociedad Americana de Geriatría . 63 (11): 2227–2246. doi : 10.1111 / jgs.13702 . PMID 26446832 . S2CID 38797655 .
- ^ Bain KT (junio de 2006). "Manejo del insomnio crónico en personas mayores". Soy J. Geriatr Pharmacother . 4 (2): 168–92. doi : 10.1016 / j.amjopharm.2006.06.006 . PMID 16860264 .
- ↑ Joya FL, Kripke DF, Loving RT, Dawson A (2009). "Metanálisis de hipnóticos e infecciones: eszopiclona, ramelteon, zaleplon y zolpidem" . J. Clin. Sleep Med . 5 (4): 377–83. doi : 10.5664 / jcsm.27552 . PMC 2725260 . PMID 19968019 .
- ^ Kripke, DF (febrero de 2016). "Riesgo de mortalidad de los hipnóticos: fortalezas y límites de la evidencia" (PDF) . Seguridad de los medicamentos . 39 (2): 93-107. doi : 10.1007 / s40264-015-0362-0 . PMID 26563222 . S2CID 7946506 .
- ^ a b c d e f g h i j k l m n Rxlist (26 de octubre de 2016). "Lunesta" . Archivado desde el original el 5 de diciembre de 2008 . Consultado el 15 de abril de 2017 .
- ^ Joya, FL; Kripke, DF; Amoroso, RT; Dawson, A; Kline, LE (2009). "Metanálisis de hipnóticos e infecciones: eszopiclona, ramelteon, zaleplon y zolpidem" . Revista de Medicina Clínica del Sueño . 5 (4): 377–383. doi : 10.5664 / jcsm.27552 . PMC 2725260 . PMID 19968019 .
- ↑ a b Brielmaier BD (enero de 2006). "Eszopiclone (Lunesta): un nuevo agente hipnótico no benzodiazepínico" . Proc (Bayl Univ Med Cent) . 19 (1): 54–9. doi : 10.1080 / 08998280.2006.11928127 . PMC 1325284 . PMID 16424933 .
- ^ "Información de prescripción de Lunesta en Drugs @ FDA" (PDF) . Consultado el 22 de mayo de 2014 .
- ^ Forrester MB (octubre de 2007). "Ingestiones de eszopiclona informadas a los centros de control de intoxicaciones de Texas, 2005 2006". Hum Exp Toxicol . 26 (10): 795–800. doi : 10.1177 / 0960327107084045 . PMID 18025051 . S2CID 25102558 .
- ^ "Sobredosis de zopiclona" . MHRA . Agencia Reguladora de Medicamentos y Productos Sanitarios. Archivado desde el original el 6 de diciembre de 2014.CS1 maint: bot: original URL status unknown (link) (Archivo del 6 de diciembre de 2014)
- ^ Jufe GS (julio-agosto de 2007). "[Nuevos hipnóticos: perspectivas desde la fisiología del sueño]". Vértice . 18 (74): 294–9. PMID 18265473 .
- ^ Halas CJ (1 de enero de 2006). "Eszopiclona". Soy J Health Syst Pharm . 63 (1): 41–8. doi : 10.2146 / ajhp050357 . PMID 16373464 .
- ^ Najib J (abril de 2006). "Eszopiclona, un sedante-hipnótico no benzodiazepínico para el tratamiento del insomnio transitorio y crónico". Clin Ther . 28 (4): 491–516. doi : 10.1016 / j.clinthera.2006.04.014 . PMID 16750462 .
- ^ Profesor Ashton (abril de 2007). "TABLA DE EQUIVALENCIA DE BENZODIAZEPINAS" . Consultado el 21 de marzo de 2008 .
- ^ Schwartz, Lisa M .; Steven Woloshin (octubre de 2009). "Perdido en la transmisión: información de la FDA sobre medicamentos que nunca llega a los médicos" . Revista de Medicina de Nueva Inglaterra . NEJM.org. 361 (18): 1717-1720. doi : 10.1056 / NEJMp0907708 . PMID 19846841 . Archivado desde el original (en línea) el 27 de octubre de 2010 . Consultado el 6 de diciembre de 2010 .
- ^ a b "GlaxoSmithKline y Sepracor Inc. anuncian alianza internacional para la comercialización de Lunivia" . Archivado desde el original el 27 de diciembre de 2010.
- ^ COMITÉ DE MEDICAMENTOS DE USO HUMANOm RESUMEN DE OPINIÓN POSITIVA para LUNIVIA - Agencia Europea de Medicamentos / Comité de Medicamentos de Uso Humano , 23 de octubre de 2010
- ^ Sepracor Pharmaceuticals Ltd retira su solicitud de autorización de comercialización para Lunivia (eszopiclona) - Agencia Europea de Medicamentos , 15 de mayo de 2009
- ^ Exclusividad de datos y definición de un nuevo principio activo: suspensión de medicamentos genéricos que contienen escitalopram por el CHMP - Bird and Bird Commercial Law 23 de abril de 2010
Enlaces externos [ editar ]
- "Eszopiclona" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.