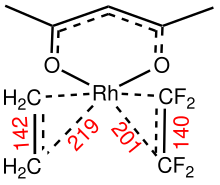Complejo de alqueno de metal de transición
En química organometálica , un complejo de alqueno de metal de transición es un compuesto de coordinación que contiene uno o más ligandos de alqueno . Dichos compuestos son intermedios en muchas reacciones catalíticas que convierten alquenos en otros productos orgánicos. [1]
El monoalqueno más simple es el eteno . Se conocen muchos complejos de eteno, incluida la sal de Zeise (ver figura), Rh 2 Cl 2 (C 2 H 4 ) 4 , Cp * 2 Ti (C 2 H 4 ) y el homoléptico Ni (C 2 H 4 ) 3 . El monoalqueno sustituido incluye el cicloocteno cíclico , como se encuentra en el dímero de clorobis (cicloocteno) rodio . Los alquenos con grupos aceptores de electrones comúnmente se unen fuertemente a metales de baja valencia. Ejemplos de tales ligandos son TCNE ,tetrafluoroetileno , anhídrido maleico y ésteres de ácido fumárico . Estos aceptores forman aductos con muchos metales de valencia cero. [1]
El butadieno , el ciclooctadieno y el norbornadieno son agentes quelantes bien estudiados. Los trienos e incluso algunos tetraenos pueden unirse a metales a través de varios centros de carbono adyacentes. Los ejemplos comunes de tales ligandos son cicloheptatrieno y ciclooctatetraeno . La unión a menudo se denota mediante el formalismo de hapticidad . Los cetoalquenos son tetrahapto ligandos que estabilizan metales de baja valencia altamente insaturados como se encuentran en (bencilidenoacetona) hierro tricarbonilo y tris (dibencilidenoacetona) dipaladio (0) .
La unión entre los alquenos y los metales de transición se describe mediante el modelo Dewar-Chatt-Duncanson , que implica la donación de electrones en el orbital pi del alqueno a los orbitales vacíos del metal. Esta interacción se ve reforzada por el enlace inverso que implica compartir electrones en otros orbitales metálicos en el nivel de antienlazamiento pi vacío en el alqueno. Los primeros metales de bajo estado de oxidación (Ti (II), Zr (II), Nb (III), etc.) son fuertes donantes de pi, y sus complejos de alquenos se describen a menudo como metalaciclopropanos. El tratamiento de tales especies con ácidos da lugar a los alcanos. Metales tarde (Ir (I), Pt (II)), que son más pobres pi-donantes, tienden a participar el alqueno como un ácido de Lewis - base de Lewis interacción. Del mismo modo, C 2 F 4es un aceptor de pi más fuerte que el C 2 H 4 , como se refleja en las distancias de enlace metal-carbono. [2]
La barrera para la rotación del alqueno alrededor del vector M-centroide es una medida de la fuerza del enlace pi del M-alqueno. Los complejos de baja simetría son adecuados para el análisis de estas barreras rotacionales asociadas con el enlace metal-eteno En Cp Rh (C 2 H 4 ) (C 2 F 4 ), se observa que el ligando de eteno rota con una barrera cercana a 12 kcal / mol pero no se observa rotación para aproximadamente el enlace Rh-C 2 F 4 . [3]
Los ligandos de alqueno pierden gran parte de su carácter insaturado tras la complejación. Lo más famoso es que el ligando de alqueno sufre una inserción migratoria , en la que es atacado intramolecularmente por ligandos de alquilo e hidruro para formar nuevos complejos de alquilo. Los complejos de alquenos catiónicos son susceptibles de ser atacados por nucleófilos. [1]