 | |
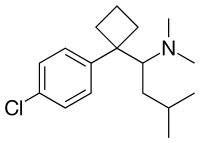
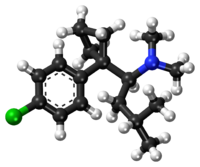 Sibutramina (arriba), ( S ) - (-) - sibutramina (abajo) | |
| Datos clinicos | |
|---|---|
| Nombres comerciales | Meridia, otros |
| Otros nombres | BTS-54524 |
| AHFS / Drugs.com | Monografía |
| MedlinePlus | a601110 |
Categoría de embarazo |
|
| Vías de administración | Oral ( cápsulas ) |
| Código ATC | |
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Biodisponibilidad | Absorción 77%, considerable metabolismo de primer paso |
| Enlace proteico | 97%, (94% para sus metabolitos desmetil, M 1 y M 2 ) |
| Metabolismo | Hepático ( mediado por CYP3A4 ) |
| Vida media de eliminación | 1 hora (sibutramina), 14 horas (M 1 ) y 16 horas (M 2 ) |
| Excreción | Orina (77%), heces (8%) |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEMBL | |
| Tablero CompTox ( EPA ) |
|
| Tarjeta de información ECHA | 100.130.097 |
| Datos químicos y físicos | |
| Fórmula | C 17 H 26 Cl N |
| Masa molar | 279,85 g · mol −1 |
| Modelo 3D ( JSmol ) |
|
Sonrisas
| |
InChI
| |
| (verificar) | |
La sibutramina , que anteriormente se vendía bajo la marca Meridia entre otros, es un supresor del apetito que ha sido descontinuado en muchos países. Hasta 2010, se comercializó ampliamente y se recetó como un complemento en el tratamiento de la obesidad junto con la dieta y el ejercicio . Se ha asociado con un aumento de eventos cardiovasculares y accidentes cerebrovasculares y se ha retirado del mercado en varios países y regiones, incluidos Australia , [1] Canadá , [2] China , [3] elUnión Europea , [4] Hong Kong , [5] la India , [6] México , Nueva Zelanda , [7] el Filipinas , [8] Tailandia , [9] el Reino Unido , [10] y el Estados Unidos . [11] Sin embargo, el medicamento sigue estando disponible en algunos países. [12]
La sibutramina fue desarrollada originalmente en 1988 por Boots en Nottingham , Reino Unido, [13] y comercializada por Knoll Pharmaceuticals después de que BASF / Knoll AG comprara la División de Investigación de Boots en 1995, y fue fabricada y comercializada recientemente por Abbott Laboratories antes de su retirada de la mayoría de los mercados. . Se ha vendido bajo una variedad de marcas como Reductil, Meridia, Siredia y Sibutrex. Está clasificada como sustancia controlada de la Lista IV en los Estados Unidos .
Usos médicos [ editar ]
La sibutramina se ha utilizado para producir supresión del apetito con el fin de lograr la pérdida de peso en el tratamiento de pacientes con obesidad.
Contraindicaciones [ editar ]
La sibutramina está contraindicada en pacientes con:
- Condiciones psiquiátricas como bulimia nerviosa , anorexia nerviosa , depresión grave o manía preexistente
- Pacientes con antecedentes o predisposición al abuso de drogas o alcohol.
- Hipersensibilidad al fármaco o cualquiera de los ingredientes inactivos.
- Pacientes menores de 18 y mayores de 65 años [14]
- Tratamiento concomitante con un inhibidor de la MAO , antidepresivos u otros fármacos de actividad centralizada , en particular otros anoréticos.
- Historia de enfermedad arterial periférica
- Hipertensión que no está suficientemente controlada (p. Ej.,> 145/90 mmHg), precaución en la hipertensión controlada
- Hipertensión pulmonar existente
- Daño existente en las válvulas cardíacas, enfermedad coronaria, insuficiencia cardíaca congestiva, arritmias graves, infarto de miocardio previo
- Antecedentes de enfermedad de las arterias coronarias (p. Ej., Angina, antecedentes de infarto de miocardio), insuficiencia cardíaca congestiva, taquicardia, enfermedad arterial periférica oclusiva, arritmia o enfermedad cerebrovascular (accidente cerebrovascular o accidente isquémico transitorio (AIT)) [14]
- Accidente cerebrovascular o ataque isquémico transitorio (AIT)
- Hipertiroidismo (glándula tiroides hiperactiva)
- Glaucoma de ángulo cerrado
- Trastornos convulsivos
- Agrandamiento de la glándula prostática con retención urinaria (contraindicación relativa)
- Feocromocitoma
- Mujeres embarazadas y lactantes (contraindicación relativa)
Efectos secundarios [ editar ]
Se ha observado un mayor número de eventos cardiovasculares en personas que toman sibutramina en comparación con el grupo de control (11,4% frente a 10,0%). [15] En 2010, la FDA señaló las preocupaciones de que la sibutramina aumenta el riesgo de ataques cardíacos y accidentes cerebrovasculares en pacientes con antecedentes de enfermedad cardiovascular. [15]
Los efectos secundarios que se encuentran con frecuencia son: boca seca, paradójicamente aumento del apetito, náuseas , sabor extraño en la boca , malestar estomacal, estreñimiento, dificultad para dormir, mareos, somnolencia, calambres / dolor menstrual, dolor de cabeza, rubor o dolor articular / muscular.
La sibutramina puede aumentar sustancialmente la presión arterial y la frecuencia cardíaca en algunos pacientes. [16] Por tanto, es necesario realizar un seguimiento periódico.
Los siguientes efectos secundarios son poco frecuentes pero graves y requieren atención médica inmediata: arritmias cardíacas , parestesia , cambios mentales / anímicos (p. Ej., Excitación, inquietud, confusión, depresión, pensamientos suicidas raros ).
Los síntomas que requieren atención médica urgente son convulsiones , problemas para orinar, hematomas o sangrado anormales, melena , hematemesis , ictericia , fiebre y escalofríos , dolor de pecho , hemiplejía , visión anormal, disnea y edema .
Actualmente, no se ha observado ningún caso de hipertensión pulmonar . (La fenfluramina, del combo "Fen-Phen" de la década de 1990, forzó la liberación excesiva de neurotransmisores, una acción diferente. La fentermina no estuvo involucrada en los problemas cardíacos raros, pero clínicamente significativos, de la fenfluramina).
Interacciones [ editar ]
La sibutramina tiene una serie de interacciones clínicamente significativas. No está indicado el uso concomitante de sibutramina e inhibidores de la monoaminooxidasa (IMAO, como la selegilina ), ya que puede aumentar el riesgo de síndrome serotoninérgico , una reacción adversa poco frecuente pero grave . [17] La sibutramina no debe tomarse dentro de las dos semanas posteriores a la interrupción o el inicio de un IMAO. Tomar sibutramina y ciertos medicamentos utilizados en el tratamiento de las migrañas , como ergolinas y triptanos , así como opioides., también puede aumentar el riesgo de síndrome serotoninérgico, al igual que el uso de más de un inhibidor de la recaptación de serotonina al mismo tiempo. [17]
El uso concomitante de sibutramina y fármacos que inhiben el CYP3A4 , como ketoconazol y eritromicina , puede aumentar los niveles plasmáticos de sibutramina. [18] La sibutramina no afecta la eficacia de la anticoncepción hormonal . [17]
Farmacología [ editar ]
Farmacodinámica [ editar ]
| Compuesto | SERT | NETO | DAT |
|---|---|---|---|
| Sibutramina | 298-2,800 | 350–5 451 | 943–1,200 |
| Desmetilsibutramina | 15 | 20 | 49 |
| ( R ) -desmetilsibutramina | 44 | 4 | 12 |
| ( S ) -desmetilsibutramina | 9.200 | 870 | 180 |
| Didesmetilsibutramina | 20 | 15 | 45 |
| ( R ) -didesmetilsibutramina | 140 | 13 | 8,9 |
| ( S ) -didesmetilsibutramina | 4.300 | 62 | 12 |
| Los valores son K i (nM). | |||
La sibutramina es un inhibidor de la recaptación de monoaminas (IRM) que, en humanos, reduce la recaptación de norepinefrina (en ~ 73%), serotonina (en ~ 54%) y dopamina (en ~ 16%), [21] aumentando así los niveles de estas sustancias en las hendiduras sinápticas y que ayudan a mejorar la saciedad ; Se cree que la acción serotoninérgica, en particular, influye en el apetito. Los agentes anoréxicos más antiguos , como la anfetamina y la fenfluramina, fuerzan la liberación de estos neurotransmisores en lugar de afectar su recaptación. [22]
A pesar de tener un mecanismo de acción similar a los antidepresivos tricíclicos , la sibutramina no ha logrado demostrar propiedades antidepresivas en estudios con animales. Fue aprobado por la Administración de Drogas y Alimentos de los Estados Unidos (FDA) en noviembre de 1997 [23] para el tratamiento de la obesidad.
Se informa que la sibutramina es un profármaco para dos metabolitos activos , desmetilsibutramina (M1; BTS-54354) y didesmetilsibutramina (M2; BTS-54505), con una potencia mucho mayor que las resonancias magnéticas. [24] [25]
A diferencia de otros supresores del apetito serotonérgico como fenfluramina , sibutramina y sus metabolitos tienen solamente bajo y probablemente inconsecuente afinidad para la 5-HT 2B receptor . [21]
Farmacocinética [ editar ]
La sibutramina se absorbe bien en el tracto gastrointestinal (77%), pero sufre un considerable metabolismo de primer paso , lo que reduce su biodisponibilidad. El fármaco en sí alcanza su nivel máximo en plasma después de 1 hora y también tiene una vida media de 1 hora. La sibutramina es metabolizada por la isoenzima CYP3A4 del citocromo P450 en dos aminas primarias y secundarias farmacológicamente activas.(denominados metabolitos activos 1 y 2) con vidas medias de 14 y 16 horas, respectivamente. Las concentraciones plasmáticas máximas de los metabolitos activos 1 y 2 se alcanzan después de tres a cuatro horas. La siguiente vía metabólica da como resultado principalmente dos metabolitos conjugados e hidroxilados inactivos (llamados metabolitos 5 y 6). Los metabolitos 5 y 6 se excretan principalmente en la orina.
Química [ editar ]
La sibutramina se ha utilizado habitualmente en forma de sal monohidrato de hidrocloruro .
Detección en fluidos corporales [ editar ]
La sibutramina y sus dos metabolitos activos N- desmetilados pueden medirse en biofluidos mediante cromatografía líquida ( espectrometría de masas) . Los niveles plasmáticos de estas tres especies son por lo general en el 1-10 μ g / intervalo de L en personas sometidas a terapia con el fármaco. El compuesto original y norsibutramine a menudo no son detectables en la orina, pero dinorsibutramine está generalmente presente en concentraciones de> 200 μ g / L. [26] [27] [28]
Sociedad y cultura [ editar ]
Aprobación reglamentaria [ editar ]
Se están realizando estudios sobre informes de muerte súbita, insuficiencia cardíaca , insuficiencia renal y problemas gastrointestinales. A pesar de una petición de 2002 de la ONG Public Citizen , fundada por Ralph Nader , [29] la FDA no hizo ningún intento de retirar el medicamento, pero fue parte de una audiencia en el Senado en 2005. [30] De manera similar, David Graham , "denunciante" de la FDA, testificó ante una audiencia del Comité de Finanzas del Senado que la sibutramina puede ser más peligrosa que las condiciones para las que se usa. [31]
Entre enero de 2003 y noviembre de 2005, un gran estudio aleatorizado y controlado "Sibutramine Cardiovascular OUTcomes" (SCOUT) con 10,742 pacientes examinó si la sibutramina administrada dentro de un programa de control de peso reduce el riesgo de complicaciones cardiovasculares en personas con alto riesgo de enfermedad cardíaca y concluyó que el uso de silbutramina tenía un RR de 1,16 para el resultado primario (compuesto de IM no fatal, ACV no fatal, paro cardíaco y muerte CV). [32]
En un artículo disidente, "Sibutramina: desaparecida, pero no olvidada", David Haslam (presidente del Foro Nacional de Obesidad ) dice que el estudio SCOUT tiene fallas ya que solo cubrió a pacientes de alto riesgo y no consideró a los pacientes obesos que no tienen complicaciones cardiovasculares o contraindicaciones similares [33]
El 21 de enero de 2010, la Agencia Europea de Medicamentos recomendó la suspensión de las autorizaciones de comercialización de la sibutramina basándose en los resultados del estudio SCOUT. [34]
En agosto de 2010, la FDA agregó una nueva contraindicación para pacientes mayores de 65 años debido al hecho de que los estudios clínicos de sibutramina no incluyeron un número suficiente de dichos pacientes. [14]
Abbott Laboratories anunció el 8 de octubre de 2010 que está retirando la sibutramina del mercado estadounidense bajo la presión de la FDA, citando preocupaciones sobre la eficacia mínima junto con un mayor riesgo de eventos cardiovasculares adversos. [35]
Productos falsificados para adelgazar [ editar ]
El 22 de diciembre de 2008, la Administración de Drogas y Alimentos de los Estados Unidos emitió una alerta a los consumidores que mencionaban 27 productos diferentes comercializados como " suplementos dietéticos " para adelgazar, que contienen cantidades no reveladas de sibutramina de manera ilegal. [36] [37] En marzo de 2009, Dieter Müller et al. publicó un estudio de casos de intoxicación por sibutramina de " suplementos herbales " chinos similares vendidos en Europa, que contienen hasta el doble de la dosis del medicamento con licencia legal. [38]
La FDA retiró del mercado 34 productos adicionales el 22 de abril de 2009, lo que subraya aún más los riesgos asociados con los "suplementos herbales" no regulados para las personas desprevenidas. Esta preocupación es especialmente relevante para aquellos con condiciones médicas subyacentes incompatibles con adulterantes farmacéuticos no declarados. [39] En enero de 2010, se emitió una alerta similar por versiones falsificadas del medicamento de venta libre para bajar de peso que Alli vendía a través de Internet. En lugar del ingrediente activo orlistat , los medicamentos falsificados contienen sibutramina y en concentraciones al menos el doble de la cantidad recomendada para perder peso. [40]
En marzo de 2010, Health Canada informó al público que se había encontrado en el mercado una "dieta natural a base de hierbas" ilegal que contenía sibutramina, que es un medicamento recetado en Canadá, sin incluir la sibutramina como ingrediente. [41] En octubre de 2010, la FDA notificó a los consumidores que "Slimming Beauty Bitter Orange Slimming Capsules contiene el ingrediente farmacéutico activo sibutramina, un medicamento de venta con receta que es un estimulante. La sibutramina no figura en la etiqueta del producto". [42]
En octubre de 2010, la MHRA del Reino Unido emitió una advertencia con respecto al "té Payouji" y las "Cápsulas delgadas de Pai You Guo" que contenían cantidades no declaradas de sibutramina. [43]
El 30 de diciembre de 2010, la FDA emitió una advertencia con respecto a los productos dietéticos "Fruta Planta", que se encontró que contenían cantidades no declaradas de sibutramina. El retiro declaró que "NO existe una fórmula SEGURA en el mercado estadounidense y que todas las versiones de Fruta Planta contienen sibutramina. Todas las versiones de la fórmula NO SON SEGURAS y no deben comprarse de ninguna fuente". [44]
Se ha descubierto que algunos productos ilegales para adelgazar importados a Irlanda contienen sibutramina. [45] [46] Se han planteado preocupaciones similares en Australia, donde se ha descubierto que los suplementos importados ilegalmente contienen sibutramina, lo que ha provocado alertas públicas de la Administración de Productos Terapéuticos de Australia . [47]
En octubre de 2011, la FDA advirtió que 20 marcas de suplementos dietéticos estaban contaminadas con sibutramina. [48] En un estudio de 2018, la FDA encontró aditivos sintéticos, incluida la sibutramina, en más de 700 suplementos dietéticos comercializados como "remedios naturales", "tradicionales" o "a base de hierbas". [49]
Referencias [ editar ]
- ^ "Sibutramina (Reductil) - retirada en Australia" . Administración de Productos Terapéuticos, Departamento de Salud, Gobierno de Australia. 2010 . Consultado el 6 de octubre de 2014 .
- ^ Health Canada aprobó información de seguridad importante sobre MERIDIA (clorhidrato de sibutramina monohidrato) : Asunto: Retirada voluntaria de las cápsulas de Meridia (sibutramina) del mercado canadiense.
- ^ "Notificación de terminación de producción, venta y uso de preparaciones de sibutramina y su ingrediente farmacéutico activo" . sda.gov en la República Popular de China. 30 de octubre de 2010 . Consultado el 21 de mayo de 2011 .
- ^ (en alemán) Sibutramin-Vertrieb in der Europäischen Union ausgesetzt [1] . Abbott Laboratories en Alemania. Comunicado de prensa 2010-01-21. Consultado el 27 de enero de 2010.
- ^ "Baja del registro de productos farmacéuticos que contienen sibutramina" (Comunicado de prensa). info.gov en Hong Kong. 2 de noviembre de 2010 . Consultado el 8 de noviembre de 2010 .
- ^ "Medicamentos prohibidos" (Comunicado de prensa). Ministerio de Salud y Bienestar Familiar. 10 de febrero de 2011 . Consultado el 15 de marzo de 2011 .
- ^ "Retirada de sibutramina (Reductil) en Nueva Zelanda" (Comunicado de prensa). MedSafe en Nueva Zelanda. 11 de octubre de 2010 . Consultado el 6 de noviembre de 2012 .
- ^ "La FDA advierte a los vendedores en línea de píldoras adelgazantes prohibidas" . 12 de enero de 2014 . Consultado el 20 de febrero de 2014 .
- ^ "La FDA tailandesa revela la retirada voluntaria de la sibutramina del mercado tailandés" (PDF) (Comunicado de prensa). Administración de Alimentos y Medicamentos de Tailandia. 20 de octubre de 2010 . Consultado el 22 de diciembre de 2010 .
- ^ "La sibutramina de drogas de la obesidad superior está suspendida" . BBC News . 2010-01-22 . Consultado el 22 de enero de 2010 .
- ^ Rockoff JD, Dooren JC (8 de octubre de 2010). "Abbott saca Meridia de medicamentos dietéticos de los estantes de Estados Unidos" . El Wall Street Journal . Consultado el 8 de octubre de 2010 .
- ^ "Sibutramina - Drugs.com" . drugs.com .
- ^ Buckett WR, Thomas PC, Luscombe GP (1988). "La farmacología del clorhidrato de sibutramina (BTS 54 524), un nuevo antidepresivo que induce una rápida regulación negativa noradrenérgica". Progreso en Neuro-Psicofarmacología y Psiquiatría Biológica . 12 (5): 575–84. doi : 10.1016 / 0278-5846 (88) 90003-6 . PMID 2851857 . S2CID 24787523 .
- ^ a b c "Actualización de seguridad de medicamentos de la FDA de agosto de 2010" . fda.gov .
- ^ a b "Comunicación temprana sobre una revisión de seguridad en curso de Meridia (clorhidrato de sibutramina)" . Administración de Drogas y Alimentos de los Estados Unidos. 1 de febrero de 2010. Archivado desde el original el 6 de enero de 2012.
- ↑ Siebenhofer A, Jeitler K, Horvath K, Berghold A, Posch N, Meschik J, Semlitsch T (2016). "Efectos a largo plazo de los fármacos reductores de peso en pacientes hipertensos". La base de datos Cochrane de revisiones sistemáticas . 2016 : CD007654. doi : 10.1002 / 14651858.CD007654.pub4 . PMID 26934640 .
- ^ a b c "Efectos secundarios de Meridia e interacciones farmacológicas" . RxList.com. 2007 . Consultado el 29 de abril de 2007 .
- ^ (en portugués) Cloridrato de sibutramina monoidratado. Bula. [Clorhidrato de sibutramina monohidrato — información de la etiqueta]. Medley (2007).
- ^ Nisoli E, Carruba MO (octubre de 2000). "Una evaluación de la seguridad y eficacia de la sibutramina, un fármaco contra la obesidad con un mecanismo de acción novedoso". Reseñas de obesidad . 1 (2): 127–39. doi : 10.1046 / j.1467-789x.2000.00020.x . PMID 12119986 .
- ^ Rothman RB, Baumann MH (mayo de 2009). "Fármacos serotoninérgicos y valvulopatías" . Opinión de expertos sobre seguridad de los medicamentos . 8 (3): 317–29. doi : 10.1517 / 14740330902931524 . PMC 2695569 . PMID 19505264 .
- ^ a b "Meridia (clorhidrato de sibutramina monohidrato) Cápsulas CIV. Información de prescripción completa" (PDF) . Abbott Laboratories, North Chicago, IL 60064, EE . UU . Consultado el 6 de febrero de 2016 .
- ^ Heal DJ, Aspley S, Prow MR, Jackson HC, Martin KF, Cheetham SC (agosto de 1998). "Sibutramina: un fármaco novedoso contra la obesidad. Una revisión de la evidencia farmacológica para diferenciarlo de la d-anfetamina y la d-fenfluramina". Revista internacional de obesidad y trastornos metabólicos relacionados . 22 Supl. 1: S18-28, discusión S29. PMID 9758240 .
- ^ "FDA APRUEBA SIBUTRAMINA PARA TRATAR LA OBESIDAD" (Comunicado de prensa). EE.UU. Administración de Drogas y Alimentos . 24 de noviembre de 1997 . Consultado el 29 de abril de 2007 .
- ^ Kim KA, Song WK, Park JY (noviembre de 2009). "Asociación de polimorfismos genéticos CYP2B6, CYP3A5 y CYP2C19 con farmacocinética de sibutramina en sujetos coreanos sanos". Farmacología clínica y terapéutica . 86 (5): 511–8. doi : 10.1038 / clpt.2009.145 . PMID 19693007 . S2CID 24789264 .
- ^ Hofbauer K (2004). Farmacoterapia de la obesidad: opciones y alternativas . Boca Raton, Fla: CRC Press. ISBN 978-0-415-30321-7.
- ^ Jain DS, Subbaiah G, Sanyal M, et al. Método validado por cromatografía líquida / espectrometría de masas en tándem de ionización por electropulverización para la cuantificación simultánea de sibutramina y sus metabolitos de amina primaria y secundaria en plasma humano y su aplicación a un estudio de bioequivalencia. Comunicacion rapida Espectrometría de masas. 20: 3509-3521, 2006.
- ^ Thevis M, Sigmund G, Schiffer AK, Schänzer W. Determinación de N-desmetil- y N-bisdesmetil metabolitos de Sibutramina en análisis de control de dopaje usando cromatografía líquida-espectrometría de masas en tándem. EUR. J. Mass Spec. 12: 129-136, 2006.
- ^ R. Baselt, Disposición de fármacos y productos químicos tóxicos en el hombre , octava edición, Publicaciones biomédicas, Foster City, CA, 2008, págs. 1426-1427.
- ^ Wolfe SM, Sasich LD, Barbehenn E (19 de marzo de 2002). "Petición a la FDA para prohibir la sibutramina de drogas dietéticas (MERIDIA) (Publicación HRG # 1613)" . Ciudadano público . Consultado el 29 de abril de 2007 .
- ^ Japsen B (13 de marzo de 2005). "La FDA sopesa la decisión sobre Meridia; Aviso de salud probable para el medicamento contra la obesidad de Abbott". Chicago Tribune . Chicago, Illinois. pag. 1.
- ^ Audiencia de 17 de noviembre de 2004. Noticia relacionada con CBS 19 de noviembre de 2004.
- ^ James WP, Caterson ID, Coutinho W, Finer N, Van Gaal LF, Maggioni AP, Torp-Pedersen C, Sharma AM, Shepherd GM, Rode RA, Renz CL (septiembre de 2010). "Efecto de la sibutramina sobre los resultados cardiovasculares en sujetos con sobrepeso y obesidad" (PDF) . La Revista de Medicina de Nueva Inglaterra . 363 (10): 905-17. doi : 10.1056 / NEJMoa1003114 . PMID 20818901 .
- ^ Haslam D (abril de 2010). "Sibutramina: desaparecido, pero no olvidado" (PDF) . Pract Diab Int . 27 (3): 96–97. doi : 10.1002 / pdi.1453 . Archivado desde el original (PDF) el 26 de julio de 2015.
- ^ "La Agencia Europea de Medicamentos recomienda la suspensión de las autorizaciones de comercialización de la sibutramina" (PDF) . Agencia Europea de Medicamentos. 21 de enero de 2010. Archivado desde el original (PDF) el 1 de abril de 2010 .
- ^ Pollack A (8 de octubre de 2010). "Abbott Labs retira Meridia del mercado" . The New York Times .
- ^ "La FDA advierte a los consumidores sobre las píldoras de pérdida de peso contaminadas" (Comunicado de prensa). Administración de Drogas y Alimentos de los Estados Unidos. 22 de diciembre de 2008.
- ^ "Preguntas y respuestas dirigidas por el consumidor sobre la iniciativa de la FDA contra los productos de pérdida de peso contaminados" . Centro de Evaluación e Investigación de Medicamentos de la Administración de Alimentos y Medicamentos de EE. UU. 22 de diciembre de 2008.
- ^ Müller D, Weinmann W, Hermanns-Clausen M (marzo de 2009). "Cápsulas adelgazantes chinas que contienen sibutramina vendidas en Internet: una serie de casos" . Deutsches Ärzteblatt International . 106 (13): 218-22. doi : 10.3238 / arztebl.2009.0218 . PMC 2680571 . PMID 19471631 .
- ^ 34 productos para bajar de peso retirados del mercado , WebMD , 22 de abril de 2009.
- ^ "Las píldoras de dieta de Alli falsas pueden suponer riesgos para la salud" . CNN.com . 23 de enero de 2010 . Consultado el 24 de enero de 2010 .
- ^ "Producto de dieta a base de hierbas plantea riesgo para el corazón" . CBC News. 26 de marzo de 2010.
- ^ "Alerta de la FDA: belleza adelgazante cápsulas adelgazantes de naranja amarga: ingrediente de fármaco no declarado" . drugs.com .
- ^ "Comunicado de prensa: Advertencia sobre el té de hierbas sin licencia Payouji y las cápsulas Pai You Guo Slim" . Agencia Reguladora de Medicamentos y Productos Sanitarios del Reino Unido . 20 de octubre de 2010. Archivado desde el original el 9 de febrero de 2012.
- ^ "PRock Marketing, LLC emite un retiro voluntario a nivel nacional de todas las fórmulas de pérdida de peso y variación de fórmulas de Reducir peso Fruta Planta / Reducir peso Suplemento dietético" . Administración de Drogas y Alimentos de los Estados Unidos. Archivado desde el original el 23 de marzo de 2012.
- ^ Papa C. "Aumentan las incautaciones de medicamentos ilegales" . The Irish Times .
- ^ "Alerta de la FDA: Cápsula adelgazante herbal Slim Xtreme: ingrediente de fármaco no declarado" . drugs.com .
- ^ "Majestuosas cápsulas de adelgazamiento: advertencia de seguridad" . Administración de bienes terapéuticos . Gobierno de Australia. 9 de noviembre de 2012.
- ^ Carroll L (19 de octubre de 2011). " Pastillas para adelgazar ' naturales' contaminadas con medicamentos recetados prohibidos" . MSNBC . Archivado desde el original el 11 de enero de 2012.
- ^ "No es de extrañar que funcione tan bien: puede haber Viagra en ese suplemento de hierbas" . NPR.org . Consultado el 14 de octubre de 2018 .
Enlaces externos [ editar ]
- Comunicado de prensa de Abbott sobre la retirada de Meridia
- Información sobre medicamentos de sibutramina del Manual Merck . Incluye información sobre la dosis y una lista completa de marcas internacionales.
- Sitio web de seguridad de productos de la Administración de Drogas y Alimentos de EE. UU. (FDA)