 | |
| Nombres | |
|---|---|
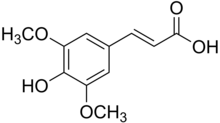
| Nombre IUPAC preferido Ácido (2 E ) -3- (4-hidroxi-3,5-dimetoxifenil) prop-2-enoico | |
| Otros nombres Ácido sinapínico Ácido sinapico Ácido 3,5-dimetoxi-4-hidroxicinámico Ácido 4-hidroxi-3,5-dimetoxicinámico | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| DrugBank | |
PubChem CID | |
| UNII | |
Tablero CompTox ( EPA ) | |
| |
| |
| Propiedades | |
| C 11 H 12 O 5 | |
| Masa molar | 224,21 g / mol |
| Punto de fusion | 203 a 205 ° C (397 a 401 ° F; 476 a 478 K) (se descompone) |
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). | |
| Referencias de Infobox | |
El ácido sinpínico , o ácido sinápico (Sinapina - Origen: L. Sinapi, sinapis, mostaza, Gr., Cf. F. Sinapine.), Es un pequeño ácido hidroxicinámico natural . Es un miembro de la familia de los fenilpropanoides . Es una matriz de uso común en espectrometría de masas MALDI . [1] [2] Es una matriz útil para una amplia variedad de péptidos y proteínas. Sirve bien como matriz para MALDI debido a su capacidad para absorber radiación láser y también para donar protones (H + ) al analito de interés.
El ácido sinápico puede formar dímeros consigo mismo (una estructura) y ácido ferúlico (tres estructuras diferentes) en las paredes de las células de los cereales y, por lo tanto, puede tener una influencia similar en la estructura de la pared celular a la de los ácidos diferúlicos . [3]
La sinapina es una amina alcaloide que se encuentra en las semillas de mostaza negra. Se considera un éster de colina del ácido sinapínico. [4]
Acontecimientos naturales
El ácido sinapínico se puede encontrar en el vino [5] y el vinagre . [6]
Metabolismo
Sinapate 1-glucosyltransferase es una enzima que usa UDP-glucosa y sinapate para producir UDP y 1-sinapoyl-D-glucosa .
Sinapoilglucosa-malato O-sinapoiltransferasa es una enzima que usa 1-O-sinapoil-beta-D-glucosa y (S) - malato para producir D- glucosa y sinapoil- (S) -malato .
Compuestos relacionados
El canolol es un compuesto fenólico que se encuentra en el aceite de canola crudo . Se produce por descarboxilación del ácido sinápico durante el tostado de la semilla de canola. [7]
Ver también
- Contenido fenólico en el vino
- Siringaldehído
- Siringol
- Ácido siríngico
- Acetosiringona
- Alcohol sinapílico
- Sinapaldehído
- Sinapina
- Canolol
Referencias
- ^ Beavis RC, Chait BT (1989). "Espectrometría de masas de desorción láser asistida por matriz utilizando radiación de 355 nm". Rapid Commun. Mass Spectrom . 3 (12): 436–9. doi : 10.1002 / rcm.1290031208 . PMID 2520224 .
- ^ Beavis RC, Chait BT (1989). "Derivados del ácido cinámico como matrices para espectrometría de masas de desorción de proteínas con láser ultravioleta". Rapid Commun. Mass Spectrom . 3 (12): 432–5. doi : 10.1002 / rcm.1290031207 . PMID 2520223 .
- ^ Bunzel M, Ralph J, Kim H, Lu F, Ralph SA, Marita JM, Hatfield RD, Steinhart H (2003). "Deshidrodímeros de sinapato y heterodímeros ferulados de sinapato en fibra dietética de cereales". J. Agric. Food Chem . 51 (5): 1427–1434. doi : 10.1021 / jf020910v . PMID 12590493 .
- ^ Tzagoloff, A. (1963). "Metabolismo de la sinapina en plantas de mostaza. I. Degradación de la sinapina en ácido sinapico y colina" . Fisiología vegetal . 38 (2): 202-206. doi : 10.1104 / pp.38.2.202 . PMC 549906 . PMID 16655775 .
- ^ Comparación de ácidos fenólicos y flavan-3-ols durante la fermentación del vino de uvas con diferentes tiempos de cosecha. Rong-Rong Tian, Qiu-Hong Pan, Ji-Cheng Zhan, Jing-Ming Li, Si-Bao Wan, Qing-Hua Zhang y Wei-Dong Huang, Molecules, 2009, 14, páginas 827-838, doi : 10.3390 / moléculas14020827
- ^ Gávez, MC; Barroso, CGA; Péez-Bustamante, JA (1994). "Análisis de compuestos polifenólicos de diferentes muestras de vinagre". Zeitschrift für Lebensmittel-Untersuchung und -Forschung . 199 : 29–31. doi : 10.1007 / BF01192948 .
- ^ Producción de canolol antioxidante a partir de una materia prima renovable a través de una descarboxilasa diseñada. Krista L.Morley, Stephan Grosse, Hannes Leischa y Peter CK Lau, Green Chem., 2013, n15, páginas 3312-3317, doi : 10.1039 / C3GC40748A