 | |
| Datos clinicos | |
|---|---|
| Nombres comerciales | Dianabol, otros |
| Otros nombres | Metandienona; Metandrostenolona; Metandrolona; Deshidrometiltestosterona; Metilboldenona; Perabol; Ciba-17309-Ba; TMV-17; NSC-51180; NSC-42722; 17α-Metil-δ 1 -testosterona; 17 $ β $ hidroxi 17 $ α $ metilandrosta 1,4 dien 3 ona; 17α-metilandrost-1,4-dien-17β-ol-3-ona |
| Vías de administración | Por vía oral , inyección intramuscular ( veterinaria ) [1] |
| Clase de droga | Andrógeno ; Esteroide anabólico |
| Código ATC | |
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Biodisponibilidad | Alto |
| Metabolismo | Hepático |
| Vida media de eliminación | 3 a 6 horas [1] [2] |
| Excreción | Orina |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| CHEMBL | |
| Tablero CompTox ( EPA ) | |
| Tarjeta de información ECHA | 100.000.716 |
| Datos químicos y físicos | |
| Fórmula | C 20 H 28 O 2 |
| Masa molar | 300,442 g · mol −1 |
| Modelo 3D ( JSmol ) |
|
Sonrisas
| |
InChI
| |
| (verificar) | |
Metandienona , también conocido como methandienone o methandrostenolone y vendido bajo el nombre de marca Dianabol entre otros, es un andrógeno y esteroides anabólicos medicación (AAS), que está en su mayoría ya no se utiliza. [3] [4] [1] [5] También se utiliza con fines no médicos para mejorar el físico y el rendimiento . [1] A menudo se toma por vía oral . [1]
Los efectos secundarios de la metandienona incluyen síntomas de masculinización como acné , aumento del crecimiento del cabello , cambios en la voz y aumento del deseo sexual , efectos estrogénicos como retención de líquidos y agrandamiento de los senos y daño hepático . [1] El fármaco es un agonista del receptor de andrógenos (AR), el objetivo biológico de los andrógenos como la testosterona y la dihidrotestosterona (DHT), y tiene fuertes efectos anabólicos.efectos y efectos androgénicos moderados . [1] También tiene efectos estrogénicos moderados. [1]
La metandienona fue desarrollada originalmente en 1955 por CIBA y comercializada en Alemania y Estados Unidos . [1] [6] [3] [7] [8] Como Dianabol, producto de CIBA, la metandienona se convirtió rápidamente en el primer AAS ampliamente utilizado entre atletas profesionales y aficionados, y sigue siendo el AAS activo por vía oral más común para uso no médico. [9] [7] [10] [11] Actualmente es una sustancia controlada en los Estados Unidos [12] y el Reino Unido [13] y sigue siendo popular entre los culturistas . La metandienona está disponible sin necesidad deprescripción médica en ciertos países como México , y también se fabrica en algunos países asiáticos . [5]
Usos médicos [ editar ]
La metandienona se aprobó y comercializó anteriormente como una forma de terapia de reemplazo de andrógenos para el tratamiento del hipogonadismo en los hombres, pero desde entonces se ha descontinuado y retirado en la mayoría de los países, incluso en los Estados Unidos . [14] [3] [5]
Se administró en dosis de 5 a 10 mg / día en hombres y 2,5 mg / día en mujeres. [15] [16] [1]
| Ruta | Medicamento | Principales marcas | Formulario | Dosis |
|---|---|---|---|---|
| Oral | Testosterona a | - | Tableta | 400 a 800 mg / día (en dosis divididas) |
| Undecanoato de testosterona | Andriol, Jatenzo | Cápsula | 40 a 80 mg / 2 a 4 veces al día (con las comidas) | |
| Metiltestosterona b | Android, Metandren, Testred | Tableta | 10 a 50 mg / día | |
| Fluoximesterona b | Halotestin, Ora-Testryl, Ultandren | Tableta | 5-20 mg / día | |
| Metandienona b | Dianabol | Tableta | 5-15 mg / día | |
| Mesterolona b | Proviron | Tableta | 25-150 mg / día | |
| Bucal | Testosterona | Striant | Tableta | 30 mg 2x / día |
| Metiltestosterona b | Metandren, Oreton Metil | Tableta | 5–25 mg / día | |
| Sublingual | Testosterona b | Testoral | Tableta | 5 a 10 mg 1 a 4 veces al día |
| Metiltestosterona b | Metandren, Oreton Metil | Tableta | 10-30 mg / día | |
| Intranasal | Testosterona | Natesto | Aerosol nasal | 11 mg 3 veces / día |
| Transdérmico | Testosterona | AndroGel, Testim, TestoGel | Gel | 25-125 mg / día |
| Androderm, AndroPatch, TestoPatch | Parche no escrotal | 2,5-15 mg / día | ||
| Testoderm | Parche escrotal | 4 a 6 mg / día | ||
| Axiron | Solución axilar | 30-120 mg / día | ||
| Androstanolona ( DHT ) | Andractim | Gel | 100 a 250 mg / día | |
| Rectal | Testosterona | Rektandron, testosterona b | Supositorio | 40 mg 2-3 veces al día |
| Inyección ( IM o SC ) | Testosterona | Andronaq, esterotato, virosterona | Suspensión acuosa | 10 a 50 mg 2 a 3 veces por semana |
| Propionato de testosterona b | Testoviron | Solución de aceite | 10 a 50 mg 2 a 3 veces por semana | |
| Enantato de testosterona | Delatestryl | Solución de aceite | 50–250 mg 1 vez / 1–4 semanas | |
| Xyosted | Autoinyector | 50-100 mg 1 vez por semana | ||
| Cipionato de testosterona | Depo-testosterona | Solución de aceite | 50–250 mg 1 vez / 1–4 semanas | |
| Isobutirato de testosterona | Depósito de agovirina | Suspensión acuosa | 50–100 mg 1 vez / 1–2 semanas | |
| Fenilacetato de testosterona b | Perandren, Androject | Solución de aceite | 50–200 mg 1 vez / 3–5 semanas | |
| Ésteres de testosterona mixtos | Sustanon 100, Sustanon 250 | Solución de aceite | 50–250 mg 1 vez / 2–4 semanas | |
| Undecanoato de testosterona | Aveed, Nebido | Solución de aceite | 750–1,000 mg 1 vez / 10–14 semanas | |
| Buciclato de testosterona a | - | Suspensión acuosa | 600–1,000 mg 1 vez / 12–20 semanas | |
| Implante | Testosterona | Testopel | Bolita | 150-1.200 mg / 3-6 meses |
| Notas: Los hombres producen alrededor de 3 a 11 mg de testosterona por día (una media de 7 mg / día en hombres jóvenes). Notas al pie: a = Nunca comercializado. b = Ya no se usa y / o ya no se comercializa. Fuentes: Ver plantilla. | ||||
Formas disponibles [ editar ]
Metandienona se proporciona en la forma de 2,5 y 5 mg por vía oral comprimidos . [17] [18] [19] [1]
Usos no médicos [ editar ]
La metandienona se usa para mejorar el físico y el rendimiento por parte de atletas competitivos , culturistas y levantadores de pesas . [1] Se dice que es el AAS más utilizado para tales fines tanto hoy como históricamente. [1]
Efectos secundarios [ editar ]
Pueden producirse efectos secundarios androgénicos como piel grasa , acné , seborrea , aumento del crecimiento del vello facial / corporal , pérdida del cabello del cuero cabelludo y virilización . [1] También pueden ocurrir efectos secundarios estrogénicos como ginecomastia y retención de líquidos . [1] Existen informes de casos de ginecomastia. [20] [21] Al igual que con otros esteroides alquilados en 17α, la metandienona presenta un riesgo de hepatotoxicidad y su uso durante períodos prolongados puede provocar daño hepático sin las precauciones adecuadas.[1]
Farmacología [ editar ]
Farmacodinámica [ editar ]
| Medicamento | Proporción a |
|---|---|
| Testosterona | ~ 1: 1 |
| Androstanolona ( DHT ) | ~ 1: 1 |
| Metiltestosterona | ~ 1: 1 |
| Metandriol | ~ 1: 1 |
| Fluoximesterona | 1: 1–1: 15 |
| Metandienona | 1: 1–1: 8 |
| Drostanolona | 1: 3–1: 4 |
| Metenolona | 1: 2–1: 30 |
| Oximetolona | 1: 2–1: 9 |
| Oxandrolona | 1: 3–1: 13 |
| Estanozolol | 1: 1–1: 30 |
| Nandrolona | 1: 3–1: 16 |
| Etilestrenol | 1: 2–1: 19 |
| Noretandrolona | 1: 1–1: 20 |
| Notas: En roedores. Notas a pie de página: a = Relación de actividad androgénica y anabólica. Fuentes: Ver plantilla. | |
La metandienona se une y activa el receptor de andrógenos (AR) para ejercer sus efectos. [22] Estos incluyen aumentos dramáticos en la síntesis de proteínas , glucogenólisis y fuerza muscular en un corto espacio de tiempo. [ cita médica necesaria ] Si bien puede ser metabolizado por la 5α-reductasa en metil-1-testosterona (17α-metil-δ 1 -DHT), un AAS más potente , el fármaco tiene una afinidad extremadamente baja por esta enzima y metil-1- por tanto, la testosterona se produce sólo en cantidades mínimas. [1] [23]Como tal, los inhibidores de la 5α-reductasa como la finasterida y la dutasterida no reducen los efectos androgénicos de la metandienona. [1] No obstante, mientras que la relación entre la actividad anabólica y androgénica de la metandienona mejora en relación con la de la testosterona , el fármaco aún posee una actividad androgénica moderada y es capaz de producir una virilización grave en mujeres y niños. [1] Como tal, solo se usa comúnmente en hombres. [1]
La metandienona es un sustrato de la aromatasa y puede metabolizarse en el estrógeno metilestradiol (17α-metilestradiol). [1] Si bien la tasa de aromatización se reduce en relación con la de la testosterona o la metiltestosterona , el estrógeno producido es resistente al metabolismo y, por lo tanto, la metandienona retiene una actividad estrogénica moderada . [1] Como tal, puede causar efectos secundarios como ginecomastia y retención de líquidos . [1] La coadministración de un antiestrógeno como unUn inhibidor de la aromatasa como el anastrozol o un modulador selectivo del receptor de estrógeno como el tamoxifeno pueden reducir o prevenir tales efectos secundarios estrogénicos. [1] La metandienona no tiene actividad progestágena . [1]
Al igual que con otros AAS 17α-alquilados, la metandienona es hepatotóxica . [1]
Farmacocinética [ editar ]
La metandienona tiene una alta biodisponibilidad oral . [1] Tiene una afinidad muy baja por la globulina fijadora de hormonas sexuales en suero humano (SHBG), aproximadamente el 10% de la de la testosterona y el 2% de la de la DHT. [24] El fármaco se metaboliza en el hígado mediante 6β- hidroxilación , 3α- y 3β- oxidación , 5β-reducción , 17- epimerización y conjugación, entre otras reacciones . [23] A diferencia de la metiltestosterona , debido a la presencia de su doble enlace C1 (2), la metandienona no produce metabolitos reducidos en 5α . [23] [1] [25] La vida media de eliminación de la metandienona es de aproximadamente 3 a 6 horas. [1] [2] Se elimina en la orina . [23]
Química [ editar ]
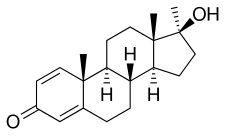
Metandienona, también conocido como 17α-metil-δ 1 -testosterona o como 17α-metilandrost-1,4-dien-17β-ol-3-ona, es un sintético androstano esteroide y un 17α-alquilados derivado de la testosterona. [6] Es una modificación de la testosterona con un grupo metilo en la posición C17α y un doble enlace adicional entre las posiciones C1 y C2. [6] El fármaco también es el derivado 17α-metilado de la boldenona (δ 1 -testosterona) y el análogo δ 1 de la metiltestosterona (17α-metiltestosterona).[6]
Detección en fluidos corporales [ editar ]
La metandienona está sujeta a una extensa biotransformación hepática por diversas vías enzimáticas. Los metabolitos urinarios primarios son detectables hasta por 3 días, y un metabolito hidroximetílico descubierto recientemente se encuentra en la orina hasta por 19 días después de una dosis oral única de 5 mg. [26] Varios de los metabolitos son exclusivos de la metandienona. Los métodos de detección en muestras de orina suelen incluir cromatografía de gases y espectrometría de masas. [27] [28]
Historia [ editar ]
La metandienona se describió por primera vez en 1955. [1] Fue sintetizada por investigadores de los laboratorios CIBA en Basilea, Suiza. CIBA solicitó una patente de EE. UU. En 1957, [29] y comenzó a comercializar el medicamento como Dianabol en 1958 en los EE . UU. [1] [30] Inicialmente se recetó para las víctimas de quemaduras y los ancianos. También se prescribió fuera de etiqueta como una mejora del rendimiento farmacéutico para los levantadores de pesas y otros atletas. [31] Los primeros en adoptarlo incluyeron jugadores de la Universidad de Oklahoma y el entrenador en jefe de los San Diego Chargers , Sid Gillman., quien administró Dianabol a su equipo a partir de 1963. [32]
Después de que se aprobó la Enmienda de Kefauver Harris en 1962, la FDA de EE. UU. Inició el proceso de revisión de DESI para garantizar la seguridad y eficacia de los medicamentos aprobados según los estándares anteriores a 1962 más indulgentes, incluido el Dianabol. [33] En 1965, la FDA presionó a CIBA para que documente más sus usos médicos legítimos y volvió a aprobar el fármaco para tratar la osteoporosis posmenopáusica y el enanismo por deficiencia pituitaria . [34] Después de que expiró el período de exclusividad de patentes de CIBA , otros fabricantes comenzaron a comercializar metandienona genérica en los Estados Unidos.
Luego de una mayor presión de la FDA, CIBA retiró Dianabol del mercado estadounidense en 1983. [1] La producción de genéricos cesó dos años después, cuando la FDA revocó la aprobación de la metandienona por completo en 1985. [1] [34] [35] El uso no médico fue prohibido en los EE. UU. en virtud de la Ley de control de esteroides anabólicos de 1990 . [36] Si bien la metandienona está controlada y ya no está disponible médicamente en los EE. UU., Se sigue produciendo y usándose médicamente en algunos otros países. [1]
Sociedad y cultura [ editar ]
Nombres genéricos [ editar ]
Metandienone es el nombre genérico de la droga y su DCI , mientras que metandienona es su BAN y métandiénone es su DCF . [6] [3] [4] [5] También se conoce como methandrostenolone y como dehydromethyltestosterone . [6] [3] [4] [1] [5] El sinónimo anterior no debe confundirse con methylandrostenolone , que es otro nombre para un AAS diferente conocido como metenolone . [3]
Nombres de marca [ editar ]
La metandienona se introdujo y anteriormente se vendía principalmente bajo la marca Dianabol. [6] [3] [4] [5] [1] También se ha comercializado bajo una variedad de otras marcas como Anabol, Averbol, Chinlipan, Danabol, Dronabol, Metanabol, Methandon, Naposim, Reforvit-B y Vetanabol entre otros. [6] [3] [4] [5] [1]
Situación legal [ editar ]
La metandienona, junto con otros AAS, es una sustancia controlada de Lista III en los Estados Unidos bajo la Ley de Sustancias Controladas . [37]
Dopaje en los deportes [ editar ]
Hay muchos casos conocidos de dopaje en deportes con metandienona por parte de atletas profesionales .
Referencias [ editar ]
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak Llewellyn W (2011). Anabolizantes . Nutrición Molecular Llc. págs. 444–454, 533. ISBN 978-0-9828280-1-4.
- ^ a b Pedro Ruiz; Eric C. Strain (2011). Abuso de sustancias de Lowinson y Ruiz: un libro de texto completo . Lippincott Williams y Wilkins. págs. 358–. ISBN 978-1-60547-277-5.
- ^ a b c d e f g h Sociedad farmacéutica suiza (2000). "Metandienona" . Index Nominum 2000: Directorio internacional de medicamentos . Taylor y Francis. pag. 660. ISBN 978-3-88763-075-1.
- ↑ a b c d e Morton IK, Hall JM (6 de diciembre de 2012). Diccionario conciso de agentes farmacológicos: propiedades y sinónimos . Springer Science & Business Media. págs. 177–. ISBN 978-94-011-4439-1.
- ^ a b c d e f g "Metandienona" . drugs.com .
- ↑ a b c d e f g h Elks J (14 de noviembre de 2014). El diccionario de drogas: datos químicos: datos químicos, estructuras y bibliografías . Saltador. págs. 781–. ISBN 978-1-4757-2085-3.
- ↑ a b Yesalis CE, Anderson WA, Buckley WE, Wright JE (1990). "Incidencia del uso no médico de esteroides anabólico-androgénicos" (PDF) . Monografía de investigación del NIDA . 102 : 97-112. PMID 2079979 .
- ^ Justo JD (1993). "¿Isométricos o esteroides? Explorando nuevas fronteras de fuerza a principios de la década de 1960" (PDF) . Revista de Historia del Deporte . 20 (1): 1–24. Archivado desde el original (PDF) el 28 de mayo de 2008.
- ^ Yesalis C, Bahrke M (2002). "Historia del Dopaje en el Deporte" (PDF) . Estudios de Deportes Internacionales . 24 : 42–76. Archivado desde el original (PDF) el 23 de noviembre de 2017 . Consultado el 14 de enero de 2017 .
- ↑ Lin GC, Erinoff L (1 de julio de 1996). Abuso de esteroides anabólicos . Editorial DIANE. pag. 29 . ISBN 978-0-7881-2969-8.
Historia de Dianabol.
- ^ Helms E (agosto de 2014). "¿Qué se puede lograr como culturista natural?" (PDF) . Revista de investigación de Alan Aragon . Alan Aragon.
- ^ "Sustancias controladas, orden alfabético" (PDF) . Administración de Control de Drogas de los Estados Unidos. Cite journal requiere
|journal=( ayuda ) - ^ "Lista de las drogas más comúnmente encontradas actualmente controladas por la legislación sobre el uso indebido de drogas" . www.gov.uk . Consultado el 14 de enero de 2017 .
- ^ Barceloux DG (3 de febrero de 2012). Toxicología médica del abuso de drogas: sustancias químicas sintetizadas y plantas psicoactivas . John Wiley e hijos. págs. 275–. ISBN 978-1-118-10605-1.
- ^ Fruehan, Alice E. (1963). "Estado actual de los esteroides anabólicos". JAMA: Revista de la Asociación Médica Estadounidense . 184 (7): 527–32. doi : 10.1001 / jama.1963.03700200049009 . ISSN 0098-7484 . PMID 13945852 .
- ^ Compendio de hojas de datos de ABPI . Pub Pharmind. 1978.
- ^ Directorio de códigos nacionales de medicamentos . Servicio de Protección al Consumidor y Salud Ambiental, Servicio de Salud Pública, Departamento de Salud, Educación y Bienestar de los EE. UU. 1982. págs. 642–.
- ^ Registro federal . Oficina del Registro Federal, Servicio de Archivos y Registros Nacionales, Administración de Servicios Generales. 18 de enero de 1983. págs. 2208–2209.
- ^ El formulario nacional ... Asociación farmacéutica estadounidense. 1974.
Tabletas disponibles - Las tabletas de metandrostenolona generalmente disponibles contienen las siguientes cantidades de metandrostenolona: 2.5 y 5 mg.
- ^ Ralph I. Dorfman (5 de diciembre de 2016). Actividad esteroidea en animales experimentales y en el hombre . Ciencia de Elsevier. págs. 70–. ISBN 978-1-4832-7300-6.
- ^ Laron, Zvi (1962). "Desarrollo mamario inducido por metandrostenolona (Dianabol)". La Revista de Endocrinología Clínica y Metabolismo . 22 (4): 450–452. doi : 10.1210 / jcem-22-4-450 . ISSN 0021-972X . PMID 14462467 .
- ^ Roselli CE (mayo de 1998). "El efecto de los esteroides anabólico-androgénicos sobre la actividad de la aromatasa y la unión del receptor de andrógenos en el área preóptica de la rata". Investigación del cerebro . 792 (2): 271–6. doi : 10.1016 / S0006-8993 (98) 00148-6 . PMID 9593936 . S2CID 29441013 .
- ↑ a b c d Schänzer W, Geyer H, Donike M (abril de 1991). "Metabolismo de la metandienona en el hombre: identificación y síntesis de metabolitos urinarios excretados conjugados, determinación de tasas de excreción e identificación por cromatografía de gases y espectrometría de masas de metabolitos bis-hidroxilados". The Journal of Steroid Biochemistry and Molecular Biology . 38 (4): 441–64. doi : 10.1016 / 0960-0760 (91) 90332-y . PMID 2031859 . S2CID 20197705 .
- ^ Saartok T, Dahlberg E, Gustafsson JA (junio de 1984). "Afinidad de unión relativa de los esteroides anabólico-androgénicos: comparación de la unión a los receptores de andrógenos en el músculo esquelético y en la próstata, así como a la globulina transportadora de hormonas sexuales". Endocrinología . 114 (6): 2100–6. doi : 10.1210 / endo-114-6-2100 . PMID 6539197 .
- ^ Kicman AT (junio de 2008). "Farmacología de los esteroides anabólicos" . Revista británica de farmacología . 154 (3): 502–21. doi : 10.1038 / bjp.2008.165 . PMC 2439524 . PMID 18500378 .
- ^ Schänzer W, Geyer H, Fusshöller G, Halatcheva N, Kohler M, Parr MK, Guddat S, Thomas A, Thevis M (2006). "Identificación y caracterización espectrométrica de masas de un nuevo metabolito a largo plazo de metandienona en orina humana". Comunicaciones rápidas en espectrometría de masas . 20 (15): 2252–8. Código Bibliográfico : 2006RCMS ... 20.2252S . doi : 10.1002 / rcm.2587 . PMID 16804957 .
- ^ Baselt R (2008). Disposición de sustancias químicas y drogas tóxicas en el hombre (8ª ed.). Foster City, CA: Publicaciones biomédicas. págs. 952–4.
- ^ Fragkaki AG, Angelis YS, Tsantili-Kakoulidou A, Koupparis M, Georgakopoulos C (mayo de 2009). "Esquemas de patrones metabólicos de esteroides androgénicos anabólicos para la estimación de metabolitos de esteroides de diseño en orina humana". The Journal of Steroid Biochemistry and Molecular Biology . 115 (1–2): 44–61. doi : 10.1016 / j.jsbmb.2009.02.016 . PMID 19429460 . S2CID 10051396 .
- ^ EE. UU. Concedió 2900398 , Wettstein A, Hunger A, Meystre C, Ehmann L, "Proceso para la fabricación de productos de deshidrogenación de esteroides", emitido el 18 de agosto de 1959, asignado a Ciba Pharmaceutical Products, Inc.
- ^ Chaney M (16 de junio de 2008). "Dianabol, el primer esteroide ampliamente utilizado, cumple 50 años" . NY Daily News . Consultado el 14 de enero de 2017 .
- ↑ Peters J (18 de febrero de 2005). "El hombre detrás del jugo" . Pizarra . ISSN 1091-2339 . Consultado el 14 de enero de 2017 .
- ↑ Quinn TJ (1 de febrero de 2009). "OTL: primer equipo de esteroides de fútbol? Los '63 Chargers" . ESPN . Consultado el 14 de enero de 2017 .
- ^ Fourcroy J (2006). "Esteroides de diseño: pasado, presente y futuro". Opinión Actual en Endocrinología, Diabetes y Obesidad . 13 (3): 306-309. doi : 10.1097 / 01.med.0000224812.46942.c3 . S2CID 87333977 .
- ↑ a b Llewellyn W (1 de enero de 2011). Anabolizantes . Nutrición Molecular Llc. ISBN 978-0-9828280-1-4.
- ↑ Roach R (14 de enero de 2017). Músculo, humo y espejos . AuthorHouse. ISBN 978-1-4670-3840-9.
- ^ División de control de desvío. "Implementación de la Ley de Control de Esteroides Anabólicos de 2004" . Departamento de Justicia de los Estados Unidos . Consultado el 14 de enero de 2017 .
- ^ Karch SB (21 de diciembre de 2006). Manual de abuso de drogas (segunda ed.). Prensa CRC. págs. 30–. ISBN 978-1-4200-0346-8.
[1] [2]
- ^ https://cimab-sa.com
- ^ https://hundredacresnyc.com/dianabol-d-bal-review