 | |
 | |
| Datos clinicos | |
|---|---|
| Pronunciación | mon te loo 'kast |
| Nombres comerciales | Singulair, otros |
| AHFS / Drugs.com | Monografía |
| MedlinePlus | a600014 |
| Datos de licencia |
|
Categoría de embarazo |
|
| Vías de administración | Oral |
| Clase de droga | Antagonista del receptor de leucotrienos |
| Código ATC | |
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Biodisponibilidad | 63–73% |
| Enlace proteico | 99% |
| Metabolismo | Hígado ( CYP2C8 mayor, CYP3A4 y CYP2C9 menor) [2] |
| Vida media de eliminación | 2,7–5,5 horas |
| Excreción | Biliar |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID |
|
| IUPHAR / BPS |
|
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| KEGG |
|
| CHEBI |
|
| CHEMBL |
|
| Tablero CompTox ( EPA ) |
|
| Tarjeta de información ECHA | 100.115.927 |
| Datos químicos y físicos | |
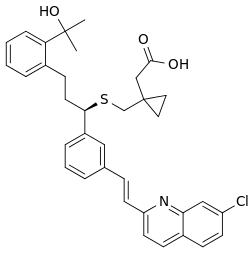
| Fórmula | C 35 H 36 Cl N O 3 S |
| Masa molar | 586,19 g · mol −1 |
| Modelo 3D ( JSmol ) |
|
| Punto de fusion | 145 a 148 ° C (293 a 298 ° F) |
Sonrisas
| |
InChI
| |
| (verificar) | |
Montelukast , vendido bajo la marca Singulair entre otros, es un medicamento utilizado en el tratamiento de mantenimiento del asma . [4] Por lo general, es menos preferido para este uso que los corticosteroides inhalados . [4] No es útil para los ataques de asma agudos . [4] Otros usos incluyen rinitis alérgica y urticaria de larga duración. [4] Para la rinitis alérgica es un tratamiento de segunda línea. [5] Cuando se usa, montelukast debe usarse en combinación con un antihistamínico.
Los efectos secundarios comunes incluyen dolor abdominal, tos y dolor de cabeza. [4] Los efectos secundarios graves pueden incluir reacciones alérgicas, como anafilaxia y eosinofilia . [4] Parece que su uso durante el embarazo es seguro. [4] Montelukast pertenece a la familia de medicamentos antagonistas de los receptores de leucotrienos . [4] Actúa bloqueando la acción del leucotrieno D4 en los pulmones, lo que reduce la inflamación y la relajación del músculo liso . [4]
Montelukast fue aprobado para uso médico en los Estados Unidos en 1998. [4] Está disponible como medicamento genérico . [6] En 2018, fue el decimoquinto medicamento más comúnmente recetado en los Estados Unidos, con más de 35 millones de recetas. [7] [8]
Usos médicos [ editar ]
Montelukast se usa para una serie de afecciones que incluyen asma , broncoespasmo inducido por el ejercicio , rinitis alérgica y urticaria . [9] Se utiliza principalmente como terapia complementaria en adultos además de los corticosteroides inhalados , si los esteroides inhalados por sí solos no producen el efecto deseado. También se utiliza para prevenir reacciones alérgicas y brotes de asma durante la administración de inmunoglobulina intravenosa . También se puede utilizar como terapia complementaria en el tratamiento sintomático de la mastocitosis . [10] Se toma por vía oral , en tabletas, tabletas masticables o en gránulos. [4]
Efectos adversos [ editar ]
Los efectos secundarios comunes incluyen diarrea, náuseas, vómitos, erupciones cutáneas leves, elevaciones asintomáticas de las enzimas hepáticas y fiebre . Los efectos secundarios poco frecuentes incluyen fatiga y malestar, cambios de comportamiento, parestesias y convulsiones, calambres musculares y hemorragias nasales. Raras (pueden afectar hasta 1 de cada 10.000 personas que toman montelukast), pero los efectos secundarios graves incluyen cambios de comportamiento (incluidos pensamientos suicidas ), angioedema , eritema multiforme y problemas hepáticos . [2]
En 2019 y 2020, se agregaron preocupaciones por reacciones neuropsiquiátricas a la etiqueta en el Reino Unido y Estados Unidos, donde las sospechas más frecuentes fueron pesadillas, depresión, insomnio (pueden afectar entre 1 de cada 100 a 1 de cada 1000 personas que toman montelukast); agresión, ansiedad y comportamiento anormal o cambios en el comportamiento (pueden afectar entre 1 de cada 1.000 a 1 de cada 10.000 personas que toman montelukast). [11] [12]
Investigación de la FDA [ editar ]
En junio de 2009, la Administración de Drogas y Alimentos de los Estados Unidos (FDA) concluyó una revisión sobre la posibilidad de efectos secundarios neuropsiquiátricos con los medicamentos moduladores de leucotrienos. [13] Aunque los ensayos clínicos solo revelaron un mayor riesgo de insomnio , la vigilancia posterior a la comercialización mostró que los medicamentos están asociados con un posible aumento de la conducta suicida y otros efectos secundarios como agitación , agresión , ansiedad , alteraciones del sueño y alucinaciones , depresión, irritabilidad , inquietud ytemblor . [13]
En septiembre de 2019, el Comité Asesor Pediátrico y el Comité Asesor de Gestión de Riesgos y Seguridad de los Medicamentos se reunieron para discutir una revisión de seguridad centrada en la pediatría de los eventos neuropsiquiátricos con montelukast. [14]
En marzo de 2020, la FDA requirió un recuadro de advertencia para montelukast para fortalecer una advertencia existente sobre el riesgo de eventos neuropsiquiátricos asociados con el fármaco a raíz de un aumento en la notificación de casos de eventos neuropsiquiátricos en el momento de las comunicaciones iniciales sobre la preocupación de FDA en 2008. [15] [16] [12] La advertencia en el recuadro advierte a los proveedores de atención médica que eviten recetar montelukast a personas con síntomas leves, particularmente a aquellas con rinitis alérgica porque hay muchos otros medicamentos antialérgicos efectivos y menos preocupantes que también son indicado para los casos leves. [15]
En el análisis de datos realizado por la FDA en comparación con los informes de casos recibidos que dependían de las afirmaciones personales de las personas, la propensión a desarrollar trastornos neuropsiquiátricos después del uso de montelukast no supera a la de los corticosteroides inhalados; y no hubo riesgos estadísticamente significativos de nuevos trastornos neuropsiquiátricos entre hombres, mujeres, pacientes de 12 años o más, pacientes con antecedentes psiquiátricos o después de la comunicación de la FDA de 2008 y los cambios en la información de prescripción que dieron a conocer la preocupación por primera vez. [dieciséis]Además, el análisis de datos realizado por la FDA también resumió sus propios hallazgos, diciendo que "la exposición a montelukast se asoció significativamente con un menor riesgo de trastorno depresivo ambulatorio tratado y los riesgos disminuidos se observaron entre pacientes con antecedentes de un trastorno psiquiátrico, en pacientes De 12 a 17 años, así como de 18 años o más, y tanto en mujeres como en hombres ". [16] "Trastorno depresivo ambulatorio tratado" se refiere a las acciones de los pacientes de concertar una cita con los psiquiatras para lidiar con sus depresiones. [dieciséis]
Interacciones farmacológicas [ editar ]
Montelukast tiene muy pocas interacciones farmacológicas. Esto se debe a la falta de afinidad fuera del objetivo hacia otros objetivos en el cuerpo donde podría ejercer un efecto. [ cita médica necesaria ] Sin embargo, es importante señalar que montelukast es un inhibidor de la enzima CYP2C8 que metaboliza los fármacos . Por tanto, es teóricamente posible que la combinación de montelukast con un sustrato CYP2C8 (p. Ej. Amodiaquina , un fármaco antipalúdico) pueda aumentar las concentraciones plasmáticas del sustrato. [17] [18]
Farmacología [ editar ]
Montelukast pertenece a la familia de medicamentos antagonistas de los receptores de leucotrienos . [4] Actúa bloqueando la acción del leucotrieno D4 en los pulmones, lo que reduce la inflamación y la relajación del músculo liso . [4]
Funciones Montelukast como un leucotrieno antagonista de los receptores ( receptores de cisteinil leucotrienos ) y por consiguiente se opone a la función de estos mediadores de la inflamación; los leucotrienos son producidos por el sistema inmunológico y sirven para promover la broncoconstricción , la inflamación, la permeabilidad microvascular y la secreción de moco en el asma y la EPOC . [19] Los antagonistas de los receptores de leucotrienos a veces se denominan coloquialmente leucostas .
Dos genes de interés son ALOX5 y LTC4S , que catalizan dos pasos principales en la ruta biosintética de los leucotrienos. [ cita requerida ]
Montelukast puede afectar la remielinización de los nervios en combinación con Pexidartinib [20] y esto puede causar beneficios clínicos o efectos secundarios.
Sociedad y cultura [ editar ]
Patentes [ editar ]
Singulair estaba cubierto por la patente estadounidense nº 5.565.473 [21] que expiró el 3 de agosto de 2012. [22] El mismo día, la FDA aprobó varias versiones genéricas de montelukast. [23]
La Oficina de Patentes y Marcas de Estados Unidos lanzó un nuevo examen de la patente que cubre Singulair el 28 de mayo de 2009. La decisión fue impulsada por el descubrimiento de referencias que no estaban incluidas en el proceso de solicitud de patente original. Las referencias fueron enviadas a través de Article One Partners , una comunidad de investigación en línea enfocada en encontrar literatura relacionada con patentes existentes. Las referencias incluían un artículo científico elaborado por un empleado de Merck sobre el ingrediente activo de Singulair. Se había presentado una patente presentada anteriormente en la misma área de tecnología. [24]Siete meses después, la Oficina de Patentes y Marcas de los Estados Unidos determinó que la patente en cuestión era válida basándose en el reexamen inicial y la nueva información proporcionada, presentando su decisión el 17 de diciembre de 2009. [25]
Usar con loratadina [ editar ]
Schering-Plough y Merck solicitaron permiso para comercializar una tableta combinada con loratadina y montelukast. Sin embargo, la FDA no ha encontrado ningún beneficio de una píldora combinada para las alergias estacionales en comparación con la combinación de los dos medicamentos, [26] y el 25 de abril de 2008 emitió una carta de no aprobación para la combinación. [27]
Nombres [ editar ]
El Mont en montelukast significa Montreal , el lugar donde Merck (MSD) desarrolló la droga. [28]
Montelukast se vende bajo una variedad de marcas que incluyen Montenaaf (NAAFCO Pharma) Montelon-10 (Apex), Montene (Square), Montair-10, Montelo-10, Monteflo y Tukast L en India , Reversair (ACI Bangladesh), Monas , Miralust, Montiva, Provair, Montril, Lumona, Lumenta, Arokast y Trilock en Bangladesh , Ventair en Nepal , Montika en Pakistán , Montelair en Brasil , Zykast en Filipinas aunque combinado con levocetirizine , Notta en Turquía , Topraz en Sudáfrica y AirOn en Venezuela .
Referencias [ editar ]
- ^ a b "Uso de montelukast (Singulair) durante el embarazo" . Drugs.com . 13 de diciembre de 2019 . Consultado el 4 de marzo de 2020 .
- ^ a b c "Singulair 10 mg comprimidos recubiertos con película: resumen de las características del producto (RCP)" . compendio de medicamentos electrónicos (emc) . Consultado el 23 de diciembre de 2018 .
- ^ "Singulair- gránulo de montelukast sódico Singulair- tableta de montelukast sódico, tableta masticable Singulair- montelukast sódico, recubierto con película" . DailyMed . 29 de abril de 2020 . Consultado el 12 de octubre de 2020 .
- ^ a b c d e f g h i j k l m "Monografía de montelukast sódico para profesionales" . Drugs.com . AHFS . Consultado el 23 de diciembre de 2018 .
- ^ Grainger, J .; Drake-Lee, A. (2006). "Montelukast en rinitis alérgica: una revisión sistemática y metanálisis". Otorrinolaringología clínica . Wiley. 31 (5): 360–367. doi : 10.1111 / j.1749-4486.2006.01276.x . ISSN 0307-7772 . PMID 17014443 . S2CID 27200676 .
- ^ Formulario nacional británico: BNF 76 (76 ed.). Prensa farmacéutica. 2018. p. 269. ISBN 9780857113382.
- ^ "El Top 300 de 2021" . ClinCalc . Consultado el 18 de febrero de 2021 .
- ^ "Montelukast - estadísticas de uso de drogas" . ClinCalc . Consultado el 18 de febrero de 2021 .
- ^ "Montelukast sódico" . La Sociedad Estadounidense de Farmacéuticos del Sistema de Salud . Consultado el 3 de abril de 2011 .
- ^ Cardet JC, Akin C, Lee MJ (octubre de 2013). "Mastocitosis: actualización sobre farmacoterapia y direcciones futuras" . Opinión de expertos sobre farmacoterapia . 14 (15): 2033-2045. doi : 10.1517 / 14656566.2013.824424 . PMC 4362676 . PMID 24044484 .
- ^ "Montelukast (Singulair): recordatorio del riesgo de reacciones neuropsiquiátricas" . Consultado el 19 de septiembre de 2019 .
- ^ a b "Singulair (montelukast) y todos los genéricos: advertencia en caja reforzada" . EE.UU. Administración de Drogas y Alimentos (FDA) . 4 de marzo de 2020 . Consultado el 4 de marzo de 2020 .
 Este artículo incorpora texto de esta fuente, que es de dominio público .
Este artículo incorpora texto de esta fuente, que es de dominio público . - ^ a b "Información actualizada sobre inhibidores de leucotrienos: Montelukast (comercializado como Singulair), Zafirlukast (comercializado como Accolate) y Zileuton (comercializado como Zyflo y Zyflo CR)" . EE.UU. Administración de Drogas y Alimentos (FDA) . 12 de junio de 2009. Archivado desde el original el 14 de noviembre de 2017 . Consultado el 1 de marzo de 2017 .
- ^ Comité consultivo pediátrico conjunto de la FDA y Comité consultivo de gestión de riesgos y seguridad de medicamentos; Aviso de reunión
- ^ a b "La FDA requiere una advertencia más estricta sobre el riesgo de eventos neuropsiquiátricos asociados con el asma y los medicamentos para la alergia Singulair y Montelukast genérico" . EE.UU. Administración de Drogas y Alimentos (FDA) (Nota de prensa). 4 de marzo de 2020 . Consultado el 4 de marzo de 2020 .
 Este artículo incorpora texto de esta fuente, que es de dominio público .
Este artículo incorpora texto de esta fuente, que es de dominio público . - ^ a b c d "La FDA requiere un recuadro de advertencia sobre los efectos secundarios graves para la salud mental del asma y el fármaco antialérgico montelukast (Singulair); aconseja restringir el uso para la rinitis alérgica" . EE.UU. Administración de Drogas y Alimentos (FDA) . 4 de marzo de 2020 . Consultado el 4 de marzo de 2020 .
 Este artículo incorpora texto de esta fuente, que es de dominio público .
Este artículo incorpora texto de esta fuente, que es de dominio público . - ^ Artesunato Amodiaquina Winthrop (artesunato, amodiaquina) [resumen de las características del producto]. Gentilly, Francia: Sanofi-aventis; Agosto de 2010. http://www.wipo.int/export/sites/www/research/en/data/sanofi/marketed_products/Artesunate_and_Amodiquine.pdf
- ^ P alemán, invernadero B, Coates C, et al. (Marzo de 2007). "Hepatotoxicidad por interacción farmacológica entre amodiaquina más artesunato y efavirenz" . Clin. Infectar. Dis . 44 (6): 889–91. doi : 10.1086 / 511882 . PMID 17304470 .
- ^ Scott JP, Peters-Golden M (septiembre de 2013). "Agentes antileucotrienos para el tratamiento de enfermedades pulmonares". Soy. J. Respir. Crit. Care Med . 188 (5): 538–544. doi : 10.1164 / rccm.201301-0023PP . PMID 23822826 .
- ^ [https: /neurosciencenews.com/remyelination-optic-nerve-17255 "Nuevas estrategias para restaurar la mielina en las células nerviosas dañadas"] Compruebe el valor ( ayuda ) . Noticias de neurociencia .
|url= - ^ 5,565,473
- ^ Detalles de patentes singulares
- ^ "La FDA aprueba las primeras versiones genéricas de Singulair para tratar el asma y las alergias" . 3 de agosto de 2012 . Consultado el 15 de agosto de 2012 .
- ^ "Estados Unidos reexamina la patente de Singulair de Merck" . Thompson Reuters. 28 de mayo de 2009.
- ^ "Merck dice que la agencia estadounidense defiende la patente de Singulair" . Thompson Reuters. 17 de diciembre de 2009.
- ^ Rubenstein, Sarah (28 de abril de 2008). "FDA estornuda en la píldora combinada Claritin-Singulair" . El Wall Street Journal .
- ^ "Schering-Plough / MERCK Pharmaceuticals recibe una carta no aprobada de la FDA para loratadina / montelukast" . Schering-Plough (Comunicado de prensa). 25 de abril de 2008. Archivado desde el original el 24 de septiembre de 2008 . Consultado el 17 de marzo de 2020 .
- ^ Li, Jie Jack (2006). "8" . Laughing Gas, Viagra y Lipitor: las historias humanas detrás de las drogas que usamos . Prensa de la Universidad de Oxford. pag. 234. ISBN 978-0195300994. Consultado el 26 de noviembre de 2017 .
Enlaces externos [ editar ]
- "Montelukast" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.
- "Montelukast sódico" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.