| Reoviridae | |
|---|---|
 | |
| Reconstrucción crio-EM de un rotavirus | |
| Clasificación de virus | |
| (no clasificado): | Virus |
| Reino : | Riboviria |
| Reino: | Orthornavirae |
| Filo: | Duplornaviricota |
| Clase: | Resentoviricetes |
| Orden: | Reovirales |
| Familia: | Reoviridae |
| Subfamilias y géneros | |
Reoviridae es una familia de virus de ARN bicatenario . Los virus miembros tienen una ampliagama de huéspedes , incluidos vertebrados , invertebrados , plantas , protistas y hongos . [1] Carecen de envolturas lipídicasy empaquetan su genoma segmentado dentro de cápsides de múltiples capas. La falta de una envoltura lipídica ha permitido obtener estructuras tridimensionales de estos virus grandes y complejos (diámetro ∼60-100 nm ), lo que revela una relación estructural y probablemente evolutiva con el cistovirus.familia de bacteriófagos . [2] Actualmente hay 97 especies en esta familia, divididas en 15 géneros en dos subfamilias. [3] Los reovirus pueden afectar el sistema gastrointestinal (como los rotavirus ) y el tracto respiratorio . [4] El nombre "reo-" es un acrónimo de " r espiratorios e nteric o rphan virus" . [5] El término " virus huérfano"se refiere al hecho de que se ha observado que algunos de estos virus no están asociados con ninguna enfermedad conocida. Aunque los virus de la familia Reoviridae se han identificado más recientemente con diversas enfermedades, todavía se usa el nombre original.
Las infecciones por reovirus ocurren a menudo en humanos, pero la mayoría de los casos son leves o subclínicos. Sin embargo, los rotavirus pueden causar diarrea severa y malestar intestinal en los niños, y los estudios de laboratorio en ratones han implicado a los ortoreovirus en la expresión de la enfermedad celíaca en individuos predispuestos. [6] El virus se puede detectar fácilmente en las heces y también se puede recuperar de las secreciones nasales o faríngeas , la orina, el líquido cefalorraquídeo y la sangre. A pesar de la facilidad para encontrar reovirus en muestras clínicas, su papel en la enfermedad humana o el tratamiento aún es incierto.
Algunos virus de esta familia, como los fitoreovirus y los orizavirus , infectan las plantas. La mayoría de los reovirus que infectan las plantas se transmiten entre plantas por medio de insectos vectores . Los virus se replican tanto en la planta como en el insecto, generalmente causando enfermedades en la planta, pero poco o ningún daño al insecto infectado. [7] : 148
Estructura
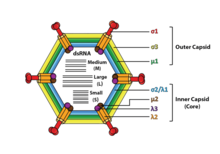
Los reovirus no tienen envoltura y tienen una cápside icosaédrica compuesta por una capa de proteína externa ( T = 13) e interna (T = 2). [1] [5] Los estudios de ultraestructura muestran que las cápsides de los viriones se componen de dos o tres capas separadas que dependen del tipo de especie. La capa más interna (núcleo) tiene una simetría icosaédrica T = 1 y está compuesta por 60 tipos diferentes de proteínas estructurales. El núcleo contiene los segmentos del genoma, cada uno de ellos codifica una variedad de estructuras enzimáticas que se requieren para la transcripción. El núcleo está cubierto por una capa de cápside T = 13 de simetría icosaédrica. Los reovirus tienen una estructura única que contiene una proteína de pico glicolizada en la superficie. [8]
Genoma
Los genomas de los virus de la familia Reoviridae contienen de 10 a 12 segmentos que se agrupan en tres categorías correspondientes a su tamaño: L (grande), M (mediano) y S (pequeño). Los segmentos varían de aproximadamente 0,2 a 3 kpb y cada segmento codifica de 1 a 3 proteínas (10 a 14 proteínas en total [1] ). Las proteínas de los virus de la familia Reoviridae se indican mediante el carácter griego correspondiente al segmento del que se tradujo (el segmento L codifica para proteínas λ, el segmento M codifica para proteínas μ y el segmento S codifica para proteínas σ). [5]
Ciclo de vida

Los virus de la familia Reoviridae tienen genomas que consisten en ARN bicatenario segmentado (ARNdc). [4] Debido a esto, la replicación ocurre exclusivamente en el citoplasma, y el virus codifica varias proteínas que son necesarias para la replicación y conversión del genoma de dsRNA en ARN de sentido positivo. [9]
El virus puede ingresar a la célula huésped a través de un receptor en la superficie celular. No se conoce el receptor, pero se cree que incluye el ácido siálico y las moléculas de adhesión de la unión (JAM). [9] El virus no está cubierto parcialmente por proteasas en el endolisosoma, donde la cápside se digiere parcialmente para permitir una mayor entrada a las células. Luego, la partícula central ingresa al citoplasma mediante un proceso aún desconocido en el que el genoma se transcribe de manera conservadora, lo que provoca un exceso de hebras de sentido positivo, que se utilizan como plantillas de ARN mensajero para sintetizar hebras de sentido negativo. [9]
El genoma del rotavirus se divide en 11 segmentos. Estos segmentos están asociados con la molécula VP1 que es responsable de la síntesis de ARN. En eventos tempranos, el proceso de selección ocurre para que la entrada de los 11 segmentos de ARN diferentes ingresen a la célula. Este procedimiento se realiza mediante ARN recién sintetizados. Este evento asegura que se reciba uno de cada uno de los 11 segmentos de ARN diferentes. En eventos tardíos, el proceso de transcripción ocurre nuevamente, pero esta vez no está limitado a diferencia de los eventos tempranos. Para los virus se requieren diferentes cantidades de ARN, por lo que durante el paso de traducción existe una maquinaria de control. Hay las mismas cantidades de segmentos de ARN pero diferentes cantidades de proteínas. La razón de esto es que los segmentos de ARN no se traducen al mismo ritmo. [7]
Las partículas virales comienzan a acumularse en el citoplasma 6 a 7 horas después de la infección. La traducción se realiza mediante exploración con fugas, supresión de la terminación y salto ribosómico . El virus sale de la célula hospedadora mediante un movimiento viral guiado por monopartitos no túbulos, movimiento de célula a célula, y existe en los cuerpos de oclusión después de la muerte celular y permanece infeccioso hasta encontrar otro hospedador. [1]
| Género | Detalles del anfitrión | Tropismo tisular | Detalles de la entrada | Detalles de lanzamiento | Sitio de replicación | Sitio de montaje | Transmisión |
|---|---|---|---|---|---|---|---|
| Aquareovirus | Vertebrados acuáticos: peces; invertebrados acuáticos: mariscos; invertebrados acuáticos: crustáceos | Ninguno | Endocitosis del receptor celular | Muerte celular | Citoplasma | Citoplasma | Difusión pasiva |
| Cardoreovirus | Crustáceos: cangrejos | Ninguno | Endocitosis del receptor celular | Muerte celular | Citoplasma | Citoplasma | Mordedura de artrópodo |
| Coltivirus | Humanos; roedores garrapatas mosquitos | Eritrocitos | Endocitosis del receptor celular | Muerte celular | Citoplasma | Citoplasma | Mordedura de artrópodo |
| Cypovirus | Insectos | Midgut; copa; gordo | Endocitosis del receptor celular | Muerte celular | Citoplasma | Citoplasma | Poliedros: oral-fecal; vertical: huevos |
| Dinovernavirus | Insectos; Mosquitos | Ninguno | Desconocido | Muerte celular | Citoplasma | Citoplasma | Desconocido |
| Fijivirus | Plants: gramineae; plants: liliacea; planthoppers | Phloem | Viral movement; mechanical inoculation | Cell death | Cytoplasm | Cytoplasm | Delphacid plant hoppers |
| Idnoreovirus | Hymenoptera | Gut | Cell receptor endocytosis | Cell death | Cytoplasm | Cytoplasm | Unknown |
| Mimoreovirus | Algae | None | Cell receptor endocytosis | Cell death | Cytoplasm | Cytoplasm | Arthropod bite |
| Mycoreovirus | Fungi | Mycelium | Cell death; cytoplasmic exchange, sporogenesis; hyphal anastomosis | Cell death; cytoplasmic exchange, sporogenesis; hyphal anastomosis | Cytoplasm | Cytoplasm | Cytoplasmic exchange, sporogenesis; hyphal anastomosis |
| Orbivirus | Vertebrates; mosquitoes; midges; gnats; sandflies; ticks | None | Cell receptor endocytosis | Cell death | Cytoplasm | Cytoplasm | Arthropod bite |
| Orthoreovirus | Vertebrates | Epithelium: intestinal; epithelium:bile duct; epithelium: lung; leukocytes; endothelium: CNS | Clathrin-mediated endocytosis | Cell death | Cytoplasm | Cytoplasm | Aerosol; oral-fecal |
| Oryzavirus | Plants: graminae, Oryza sativa; planthoppers | None | Viral movement; mechanical | Cell death | Cytoplasm | Cytoplasm | Delphacid planthoppers |
| Phytoreovirus | Oryza sativa; leafhoppers | Phloem | Viral movement; mechanical inoculation | Cell death | Cytoplasm | Cytoplasm | Leafhoppers |
| Rotavirus | Humans; vertebrates | Intestinal mucosa | Clathrin-mediated endocytosis | Cell death | Cytoplasm | Cytoplasm | Oral-fecal |
| Seadornavirus | Humans; cattle; pigs; mosquitoes | None | Cell receptor endocytosis | Cell death | Cytoplasm | Cytoplasm | Zoonosis; arthropod bite |
Reactivación de multiplicidad
La reactivación multiplicidad (MR) es el proceso mediante el cual dos o más genomas de virus, cada uno con un daño genómico inactivante, pueden interactuar dentro de una célula infectada para formar un genoma de virus viable. McClain y Spendlove [10] demostraron RM para tres tipos de reovirus después de la exposición a radiación ultravioleta. En sus experimentos, las partículas de reovirus se expusieron a dosis de luz ultravioleta que serían letales en infecciones aisladas. Sin embargo, cuando se permitió que dos o más virus inactivados infectaran células hospedadoras individuales, se produjo MR y se produjo una progenie viable. Como afirmaron, la reactivación de la multiplicidad por definición implica algún tipo de reparación. Michod y col. [11] revisó numerosos ejemplos de MR en diferentes virus y sugirió que MR es una forma común de interacción sexual en virus que proporciona el beneficio de la reparación recombinacional de los daños del genoma.
Taxonomía
La familia Reoviridae se divide en dos subfamilias [12] basadas en la presencia de una proteína de "torreta" en la cápside interna. [13] [14] De las comunicaciones de ICTV: "El nombre Spinareovirinae se utilizará para identificar la subfamilia que contiene los virus con picos o torretas y se deriva de 'reovirus' y la palabra latina 'spina' como prefijo, que significa pico, que denota la presencia de picos o torretas en la superficie de las partículas del núcleo. El término "punteado" es una alternativa a "torreta", que se utilizó en las primeras investigaciones para describir la estructura de la partícula, en particular con los cipovirus. El nombre Sedoreovirinaese utilizará para identificar la subfamilia que contiene los géneros de virus sin torretas y se deriva de 'reovirus' y la palabra latina 'sedo', que significa suave, que denota la ausencia de picos o torretas de las partículas centrales de estos virus, que tienen una morfología relativamente suave ". [15]

La familia Reoviridae se divide en las siguientes subfamilias y géneros:
- Sedoreovirinae
- Cardoreovirus
- Mimoreovirus
- Orbivirus
- Fitoreovirus
- Rotavirus
- Seadornavirus
- Espinareovirinae
- Aquareovirus
- Coltivirus
- Cypovirus
- Dinovernavirus
- Fijivirus
- Idnoreovirus
- Micoreovirus
- Orthoreovirus
- Oryzavirus
Aplicaciones terapéuticas
Aunque los reovirus son en su mayoría no patógenos en humanos, estos virus han servido como modelos experimentales muy productivos para estudios de patogénesis viral . [16] Los ratones recién nacidos son extremadamente sensibles a las infecciones por reovirus y se han utilizado como el sistema experimental preferido para estudios de patogénesis de reovirus. [2]
Se ha demostrado que los reovirus tienen propiedades oncolíticas (aniquiladoras del cáncer), lo que fomenta el desarrollo de terapias basadas en reovirus para el tratamiento del cáncer. [17] [18]
Reolysin es una formulación de reovirus ( cepa de reovirus de serotipo 3 de ortoreovirus de mamíferos [19] ) que se encuentra actualmente en ensayos clínicos para el tratamiento de varios cánceres, [20] incluidos los estudios actualmente desarrollados para investigar el papel de Reolysin combinado con otras inmunoterapias. [19]
Ver también
- Virus de ARN bicatenario
- Virus oncolítico
- Virus huérfano
Referencias
- ^ a b c d "Zona viral" . EXPASY . Consultado el 15 de junio de 2015 .
- ^ a b Guglielmi, KM; Johnson, EM; Stehle, T; Dermody, TS (2006). "Fijación y entrada celular de ortoreovirus de mamíferos". Curr Top Microbiol Immunol . 309 : 1–38. doi : 10.1007 / 3-540-30773-7_1 . PMID 16909895 .
- ^ "Taxonomía de virus: versión de 2019" . talk.ictvonline.org . Comité Internacional de Taxonomía de Virus . Consultado el 11 de mayo de 2020 .
- ^ a b c MicrobiologyBytes Archivado el 21 de mayo de 2015 en la Wayback Machine —Reovirus
- ↑ Bouziat, R; et al. (7 de abril de 2017). "La infección por reovirus desencadena respuestas inflamatorias a los antígenos de la dieta y el desarrollo de la enfermedad celíaca" . Ciencia . 356 (6333): 44–50. Código bibliográfico : 2017Sci ... 356 ... 44B . doi : 10.1126 / science.aah5298 . PMC 5506690 . PMID 28386004 .
- ^ a b Carter, John; Saunders, Venetia (2007). Virología: principios y aplicaciones . West Sussex: Wiley. ISBN 978-0-470-02386-0.
- ^ Payne S (2017). "Familia Reoviridae" . Virus : 219–226. doi : 10.1016 / B978-0-12-803109-4.00026-X .
- ^ a b c Barton, ES; Forrest, JC; Connolly, JL; Chappell, JD; Liu, Y; Schnell, FJ; Nusrat, A; Parkos, CA; Dermody, TS (9 de febrero de 2001). "La molécula de adhesión de la unión es un receptor de reovirus" . Celular . 104 (3): 441–51. doi : 10.1016 / S0092-8674 (01) 00231-8 . PMID 11239401 .
- ^ McClain ME, Spendlove RS (noviembre de 1966). "Reactivación multiplicidad de partículas de reovirus tras exposición a luz ultravioleta" . J. Bacteriol . 92 (5): 1422–9. doi : 10.1128 / JB.92.5.1422-1429.1966 . PMC 276440 . PMID 5924273 .
- ^ Michod, RE; Bernstein, H .; Nedelcu, AM (2008). "Valor adaptativo del sexo en patógenos microbianos". Infección, Genética y Evolución . 8 (3): 267–285. doi : 10.1016 / j.meegid.2008.01.002 . PMID 18295550 .
- ^ Carstens, EB (enero de 2010). "Votación de ratificación de propuestas taxonómicas al Comité Internacional de Taxonomía de Virus (2009)" . Archivos de Virología . 155 (1): 133-146. doi : 10.1007 / s00705-009-0547-x . PMC 7086975 . PMID 19960211 .
- ↑ Hill C, Booth T, et al. (1999). "La estructura de un cypovirus y la organización funcional de virus dsRNA". Biología estructural de la naturaleza . 6 (6): 565–9. doi : 10.1038 / 9347 . PMID 10360362 .
- ^ Knipe D, Howley P, et al. (2006). Campos de Virología . Filadelfia, Pensilvania: Wolters Kluwer, Lippincott Williams & Wilkins. pag. 1855. ISBN 978-0-7817-6060-7.
- ^ Attoui, Houssam; Mertens, Peter. "Plantilla de propuesta taxonómica al Comité Ejecutivo de ICTV para crear una nueva subfamilia en una familia existente" . Comité Internacional de Taxonomía de Virus . 2007.127-129V.v2.Spina-Sedoreovirinae. págs. 1–9.
- ^ Acheson, Nicholas H. Fundamentos de virología molecular . John Wiley e hijos (2011). p.234
- ^ Lal R, Harris D, Postel-Vinay S, de Bono J (octubre de 2009). "Reovirus: justificación y actualización del ensayo clínico". Curr. Opin. Mol. Ther . 11 (5): 532–9. PMID 19806501 .
- ^ Kelland, K. (13 de junio de 2012). "El virus del resfriado viaja para matar el cáncer: estudio" . Reuters . Consultado el 17 de junio de 2012 .
- ^ a b Babiker, HM; Riaz, IB; Husnain, M .; Borad, MJ (febrero de 2017). "Viroterapia oncolítica que incluye Rigvir y terapias estándar en melanoma maligno" . Viroterapia oncolítica . Dovepress, Nueva Zelanda NLM. 6 : 11-18. doi : 10.2147 / OV.S100072 . ISSN 2253-1572 . PMC 5308590 . PMID 28224120 . 101629828.
- ^ Thirukkumaran C, Morris DG (2009). "Terapia viral oncolítica con reovirus". Methods Mol. Biol . Métodos en Biología Molecular. 542 : 607–34. doi : 10.1007 / 978-1-59745-561-9_31 . ISBN 978-1-934115-85-5. PMID 19565924 .
Enlaces externos
- ICTV: Reoviridae
- Descripción de virus vegetales: Reoviridae
- ViPR: Reoviridae
- " Reoviridae " . Navegador de taxonomía NCBI . 10880.