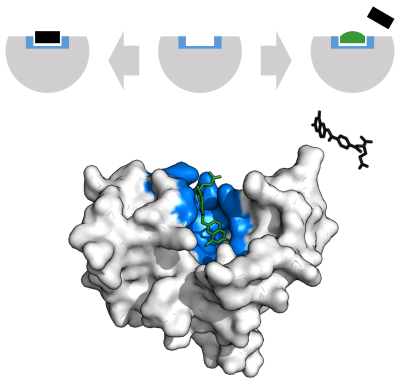
Inhibidor de enzimas
Un inhibidor enzimático es una molécula que se une a una enzima y disminuye su actividad . Al unirse a los sitios activos de las enzimas, los inhibidores reducen la compatibilidad del sustrato y la enzima y esto conduce a la inhibición de la formación de complejos Enzima-Sustrato, impidiendo la catálisis de las reacciones y disminuyendo (a veces a cero) la cantidad de producto producido por un reacción. Se puede decir que a medida que aumenta la concentración de inhibidores enzimáticos, la tasa de actividad enzimática disminuye y, por lo tanto, la cantidad de producto producido es inversamente proporcional a la concentración de moléculas inhibidoras. Dado que el bloqueo de la actividad de una enzima puede matar un patógeno o corregir un problema metabólicodesequilibrio, muchos medicamentos son inhibidores enzimáticos. También se utilizan en pesticidas . No todas las moléculas que se unen a enzimas son inhibidores; los activadores enzimáticos se unen a las enzimas y aumentan su actividad enzimática , mientras que los sustratos enzimáticos se unen y se convierten en productos en el ciclo catalítico normal de la enzima.
La unión de un inhibidor puede impedir que un sustrato entre en el sitio activo de la enzima y/o impedir que la enzima catalice su reacción. La unión del inhibidor es reversible o irreversible. Los inhibidores irreversibles normalmente reaccionan con la enzima y la modifican químicamente (p. ej., mediante la formación de enlaces covalentes ). Estos inhibidores modifican los residuos de aminoácidos clave necesarios para la actividad enzimática. Por el contrario, los inhibidores reversibles se unen de forma no covalente y se producen diferentes tipos de inhibición dependiendo de si estos inhibidores se unen a la enzima , al complejo enzima-sustrato oa ambos.
Muchas moléculas de fármacos son inhibidores de enzimas, por lo que su descubrimiento y mejora es un área activa de investigación en bioquímica y farmacología . [1] Un inhibidor enzimático medicinal a menudo se juzga por su especificidad (su falta de unión a otras proteínas) y su potencia (su constante de disociación , que indica la concentración necesaria para inhibir la enzima). Una alta especificidad y potencia aseguran que un fármaco tenga pocos efectos secundarios y, por lo tanto, baja toxicidad .
Los inhibidores de enzimas también ocurren naturalmente y están involucrados en la regulación del metabolismo . Por ejemplo, las enzimas en una ruta metabólica pueden ser inhibidas por productos aguas abajo. Este tipo de retroalimentación negativa ralentiza la línea de producción cuando los productos comienzan a acumularse y es una forma importante de mantener la homeostasis en una célula . Otros inhibidores de enzimas celulares son proteínas que se unen específicamente e inhiben un objetivo enzimático. Esto puede ayudar a controlar las enzimas que pueden dañar una célula, como las proteasas o las nucleasas . Un ejemplo bien caracterizado de esto es el inhibidor de la ribonucleasa , que se une aribonucleasas en una de las interacciones proteína-proteína más estrechas que se conocen . [2] Los inhibidores de enzimas naturales también pueden ser venenos y se utilizan como defensa contra los depredadores o como formas de matar presas.
Los inhibidores reversibles se adhieren a las enzimas con interacciones no covalentes , como enlaces de hidrógeno , interacciones hidrofóbicas y enlaces iónicos . Múltiples enlaces débiles entre el inhibidor y el sitio activo se combinan para producir una unión fuerte y específica. A diferencia de los sustratos y los inhibidores irreversibles, los inhibidores reversibles generalmente no experimentan reacciones químicas cuando se unen a la enzima y pueden eliminarse fácilmente por dilución o diálisis .
Hay cuatro tipos de inhibidores enzimáticos reversibles. Se clasifican según el efecto de variar la concentración del sustrato de la enzima sobre el inhibidor. [3] [4] [1]